
| A. | 水电离产生的H+浓度为1×10-12mol•L-1的溶液:NH4+、Na+、Cl-、CO32- | |
| B. | 能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- | |
| C. | 0.1 mol/L的NaNO3溶液中:H+、Fe2+、Cl-、SO42- | |
| D. | 含有大量Al3+的水溶液中:Na+、NH4+、HCO3-、Br- |
分析 A.水电离产生的H+浓度为1×10-12mol•L-1的溶液,为酸或碱溶液;
B.能使pH试纸变深蓝色的溶液,显碱性;
C.离子之间发生氧化还原反应;
D.离子之间相互促进水解.
解答 解:A.水电离产生的H+浓度为1×10-12mol•L-1的溶液,为酸或碱溶液,酸溶液中不能大量存在CO32-,碱溶液中不能大量存在NH4+,故A不选;
B.能使pH试纸变深蓝色的溶液,显碱性,该组离子之间不反应,可大量共存,故B选;
C.H+、Fe2+、NO3-发生氧化还原反应,不能共存,故C不选;
D.HCO3-、Al3+相互促进水解,不能共存,故D不选;
故选B.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应、复分解反应的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | m×50×18×6.02×1023 | B. | $\frac{m×6.02×1{0}^{23}}{50×18}$ | ||
| C. | $\frac{18m×6.02×1{0}^{23}}{50}$ | D. | $\frac{50×18×m}{6.02×1{0}^{23}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有Mg2+、Al3+、Clˉ,可能含有Na+,不含NH4+ | |
| B. | 一定含有Mg2+、Clˉ,不含NH4+,可能含有Na+、Al3+ | |
| C. | c (Clˉ) 为 4.00 mol•L-1,c(Al3+)为5.00 mol•L-1 | |
| D. | c (Mg2+) 为 1.00 mol•L-1,c(Na+)为 0.5mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 制备方法 | 化学共沉淀法 | 碾磨法 | 蒸着(zhuó)法 |
| 制得磁流体颗粒直径 | 大约40纳米左右 | 大于300纳米 | 2-10纳米 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
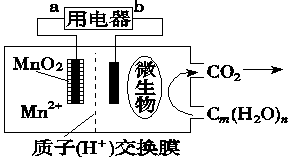
| A. | 电池工作时,电子由b流向a | |
| B. | 正极反应式为:MnO2+4H++2e-═Mn2++2H2O | |
| C. | 放电过程中,H+从负极区移向正极区 | |
| D. | 微生物所在电极区放电时发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2分解产生1molO2,转移的电子数为4NA | |
| B. | 1.00mol NaCl中,所有Na+的最外层电子总数约为8 NA | |
| C. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA | |
| D. | 标准状况下,2.24LCH4所含电子数为NA |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省德州市高二上10月月考化学试卷(解析版) 题型:选择题
N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是( )
A.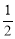 N2H4(g)+
N2H4(g)+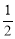 O2(g)=
O2(g)=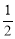 N2(g)+H2O(g) ΔH=+267 kJ·mol-1
N2(g)+H2O(g) ΔH=+267 kJ·mol-1
B.N2H4(g)+O2(g)==N2(g)+2H2O(g) ΔH =-534 kJ·mol-1
C.N2H4(g)+O2(g)==N2(g)+2H2O(g) ΔH =+534 kJ·mol-1
D.N2H4(g)+O2(g)==N2(g)+2H2O(l) ΔH =-133.5 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com