
化学用语是化学学科的特色语言,化学用语可以准确表述化学现象、变化以及本质。完成下列有关方程式。
(1)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO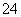 ,常用作脱氯剂,该反应的离子方程式为______________________________________________________;
,常用作脱氯剂,该反应的离子方程式为______________________________________________________;
(2)酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式:
________________________________________________________________________。
(3)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:
________________________________、________________________________________。
(4)向含有n mol 溴化亚铁的溶液中通入等物质的量的的氯气,请写出离子方程式:
_________________________________________________________________________。
科目:高中化学 来源: 题型:
某一离子反应体系有反应物和产物共以下六种:
MnO4-、H+、O2、H2O、H2O2、Mn2+,
已知该反应中的H2O2只发生如下过程: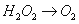
(1)该反应中的还原剂是 ,还原产物是________。
(2)KMnO4溶液随着酸性的增强氧化性不断增强,应选择_______(选填“稀硫酸”或“浓盐酸”)进行KMnO4溶液的酸化。
(3)假如反应转移了0.3mol电子,则产生的气体在标准状况下体积为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学学习中使用数轴的表示方法可收到直观、形象的效果,下列表达中正确的是( )
A.分散质微粒的大小与分散系种类的关系:
B.常温下溶液的pH其酸碱性的关系:
C.硫的化合物中化合价与其氧化性、还原性的关系:
D.Fe在Cl2中燃烧的产物与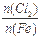 的关系:
的关系: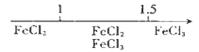
查看答案和解析>>
科目:高中化学 来源: 题型:
FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1︰1︰1时,实际参加反应的FeS与HNO3的物质的量之比为( )
A.1∶6 B.1∶7 C.2∶11 D.16∶25
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏德罗常数,下列叙述一定正确的是( )
A.标准状况下,2.24LH2O含有的质子数为 NA
B.等物质的量的氮气和氧气,都含有2NA个原子
C.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.二氧化硅能与NaOH溶液反应,又能和HF反应,属于两性氧化物
B.工业上精炼Cu,阳极用的电极材料是粗铜
C.Fe3O4既能通过化合反应得到,又能通过置换反应得到
D.周期表中的碱金属元素,从上到下,熔点依次降低
查看答案和解析>>
科目:高中化学 来源: 题型:
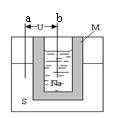
下图为钠硫高能电池的结构示意图,M为Na2O和Al2O3的混合物,电池反应为2Na+xS Na2Sx该电池的工作温度为320℃左右,下列说法错误的是
Na2Sx该电池的工作温度为320℃左右,下列说法错误的是
A.a为电池正极,b为电池负极
B.电池放电时,正极反应为xS+2e- = Sx2-
C.电池充电时,Na所在电极连接电源正极
D.M的作用为导电和隔离钠和硫
查看答案和解析>>
科目:高中化学 来源: 题型:
人体血液中存在平衡: ,使血液pH保持在7.35~7.45之间,否则就会发生酸中毒或碱中毒。已知pH随c(HCO3—)︰c(H2CO3) 变化关系如下表所示,则下列说法中不正确的是
,使血液pH保持在7.35~7.45之间,否则就会发生酸中毒或碱中毒。已知pH随c(HCO3—)︰c(H2CO3) 变化关系如下表所示,则下列说法中不正确的是
| c(HCO3—)︰c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
A.pH=7的血液中,c(HCO3—) > c(H2CO3)
B.人体发生酸中毒时,可静脉滴注一定浓度的NaHCO3溶液解毒
C.常温下将pH=7.40的血液稀释至pH=7时,c(H+)·c(OH—)一定不变
D.c(HCO3—)︰c(H2CO3)=1时,H2CO3的电离程度小于HCO3—的水解程度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com