
| A”¢SO42-ŗĶNO3-æÉÄÜĄ“×ŌĶ¬Ņ»¹¤³§ |
| B”¢Cl-ŗĶNO3-Ņ»¶ØŌŚĻąĶ¬µÄ¹¤³§ |
| C”¢Ag+ŗĶNa+æÉÄÜĄ“×ŌĶ¬Ņ»¹¤³§ |
| D”¢Na+ŗĶNO3-Ņ»¶ØĄ“×Ō²»Ķ¬µÄ¹¤³§ |


 ĒįĖÉŹī¼Ł×Üø“Ļ°ĻµĮŠ“š°ø
ĒįĖÉŹī¼Ł×Üø“Ļ°ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
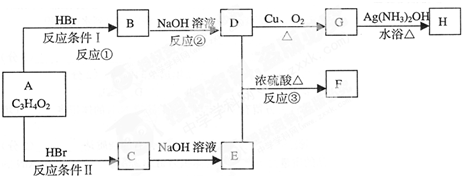
 ijĶ¬Ń§ŌŚĢ½¾æ³£¼ūĪļÖŹ×Ŗ»ÆŹ±£¬·¢ĻÖ²æ·ÖĪļÖŹ¼äæÉ“ęŌŚČēĶ¼ĖłŹ¾µÄČż½Ē×Ŗ»»¹ŲĻµ£®ŅŃÖŖ£ŗ
ijĶ¬Ń§ŌŚĢ½¾æ³£¼ūĪļÖŹ×Ŗ»ÆŹ±£¬·¢ĻÖ²æ·ÖĪļÖŹ¼äæÉ“ęŌŚČēĶ¼ĖłŹ¾µÄČż½Ē×Ŗ»»¹ŲĻµ£®ŅŃÖŖ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| AӢK+ӢNa+ӢSO42-ӢCl- |
| BӢNa+ӢNH4+ӢSO42-ӢCl- |
| CӢNa+ӢK+ӢSO32-ӢNO3- |
| DӢNa+ӢK+ӢMnO4-ӢBr- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

| A”¢ĒśĻßa±ķŹ¾ĀČĄė×Ó |
| B”¢ĒśĻßb±ķŹ¾Ģ¼ĖįøłĄė×Ó |
| C”¢ĒśĻßc±ķŹ¾ÄĘĄė×Ó |
| D”¢ĒśĻßd±ķŹ¾Ģ¼ĖįĒāøłĄė×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢C+H2OØTCO+H2 ”÷HØT+131.3KJ?mol-1 |
| B”¢C£Øs£©+H2O£Øg£©ØTCO£Øg£©+H2£Øg£©”÷H=+10.94KJ?mol-1 |
| C”¢C£Øs£©+H2O£Øl£©ØTCO£Øg£©+H2£Øg£©”÷H=+131.3KJ?mol-1 |
| D”¢C£Øs£©+H2O£Øg£©ØTCO£Øg£©+H2£Øg£©”÷H=+131.3KJ?mol- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢³£ĪĀĻĀ½«NaHSO3ŗĶNaHCO3Į½ČÜŅŗ»ģŗĻŗó£¬ČÜŅŗ³ŹÖŠŠŌ£¬Ōņ»ģŗĻŗóµÄČÜŅŗÖŠ£ŗc£ØNa+£©=c£ØHSO3-£©+c£ØHCO3-£©+2c£ØCO32-£©+2c£ØSO32-£©+c£ØOH-£© |
| B”¢³£ĪĀĻĀ½«“×ĖįÄĘ”¢ŃĪĖįĮ½ČÜŅŗ»ģŗĻŗó£¬ČÜŅŗ³ŹÖŠŠŌ£¬Ōņ»ģŗĻŗóµÄČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØCl-£©£¾c£ØCH3COOH£© |
| C”¢³£ĪĀĻĀĪļÖŹµÄĮæÅضČĻąµČµÄ¢Ł£ØNH4£©2CO3”¢¢Ś£ØNH4£©2SO4”¢¢Ū£ØNH4£©2Fe£ØSO4£©2ČżÖÖČÜŅŗÖŠc£ØNH4+£©£ŗ¢Ū£¾¢Ś£¾¢Ł |
| D”¢ĻąĶ¬Ģõ¼žĻĀ£¬pH=5µÄ¢ŁNH4ClČÜŅŗ”¢¢ŚCH3COOHČÜŅŗ”¢¢ŪĻ”ŃĪĖįČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc£ØH+£©£ŗ¢Ł£¾¢Ś£¾¢Ū |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com