
| A. | ①③ | B. | ②④ | C. | ②③ | D. | ①④ |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑧ | B. | ④⑤⑥ | C. | ①⑤⑦ | D. | ①⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 炭具有强还原性,高温下能将二氧化硅还原为硅 | |
| B. | 碳酸氢钠能与碱反应,可用作食品的蓬松剂 | |
| C. | 浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体 | |
| D. | 铝能置换出氧化铁中的铁,钢铁工业利用铝热反应冶炼铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
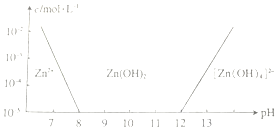 锌及其化合物有着广泛的应用.请回答有关锌及其化合物的有关问题.
锌及其化合物有着广泛的应用.请回答有关锌及其化合物的有关问题.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓盐酸具有挥发性 | B. | 浓硫酸具有脱水性 | ||
| C. | 浓硫酸和浓盐酸中的水作用而放热 | D. | 浓硫酸有吸水性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硫酸和浓盐酸混合可制氯化氢 | |
| C. | 常温下,浓硫酸可以用铝罐贮存,说明铝与浓硫酸不反应 | |
| D. | 反应CuSO4+H2S→CuS↓+H2SO4能进行,说明硫化铜既不溶于水,也不溶于稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:I2>Cl2 | B. | 每生成1 mol KIO3转移电子2 mol | ||
| C. | 该反应是置换反应 | D. | KClO3被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com