
【题目】设NA表示阿伏加德罗常数,下列叙述正确的是( )
A.100mL 12mol·L-1的浓硝酸与过量铜反应转移的电子数为0.6 NA
B.标准状况下,5.6L四氯化碳含有的分子数为0.25 NA
C.等物质的量的水与重水含有相同的质子数
D.3.4g氨气中含有的N-H键数目为0.2NA
科目:高中化学 来源: 题型:
【题目】废旧锂离子电池的回收利用意义重大,其正极废料的主要成分是![]() ,铝、炭黑及其他杂质,回收利用的流程如图1:
,铝、炭黑及其他杂质,回收利用的流程如图1:
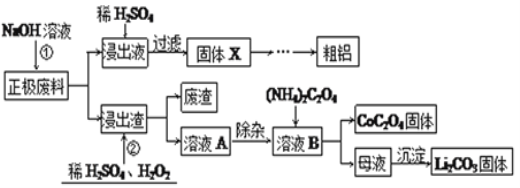
图1
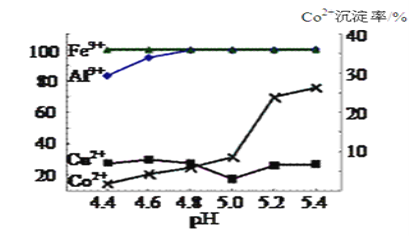
图2
已知A溶液主要的金属离子是![]() 、
、![]() ,还含有少量
,还含有少量![]() 、
、![]() 、
、![]() .
.
![]() 步骤
步骤![]() 中铝溶解的离子方程式为 ______ ,固体X的成分是 ______ ;
中铝溶解的离子方程式为 ______ ,固体X的成分是 ______ ;
![]() 步骤
步骤![]() 中
中![]() 固体溶解的化学方程式为 ______ ,该反应的还原剂是 ______ ;
固体溶解的化学方程式为 ______ ,该反应的还原剂是 ______ ;
![]() 实验表明溶液A中各种金属离子的沉淀率随pH的变化如图2,除杂时加入氨水调节溶液的pH,可除去杂质离子是 ______ ;
实验表明溶液A中各种金属离子的沉淀率随pH的变化如图2,除杂时加入氨水调节溶液的pH,可除去杂质离子是 ______ ;
![]() 母液中含量最大三种离子是 ______ ;
母液中含量最大三种离子是 ______ ;
![]() 从1000g锂离子电池正极材料
从1000g锂离子电池正极材料![]() 元素含量为
元素含量为![]() 中可回收
中可回收![]() 质量为 ______
质量为 ______ ![]() 已知回收率为
已知回收率为![]() ,
,![]() 的化学式量为74).
的化学式量为74).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25mL0.1mol·L-1某一元碱中,逐滴加入0.1mol·L-1醋酸,滴定曲线如图所示。则下列说法不正确的是

A. 该碱溶液可以溶解Al(OH)3
B. a点对应的体积值大于25mL
C. C点时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D. D点时,c(CH3COO-)+c(OH-)=c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
关于该电池的叙述不正确的是( )

A.该电池不能在高温下工作
B.电池右侧电极反应为:C6H12O6+6H2O-24e-=6CO2↑+24H+
C.放电过程中,H+通过质子交换膜向电池右侧迁移
D.在电池反应中,每消耗1mol氧气,理论上能生成CO222.4 L(标况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是
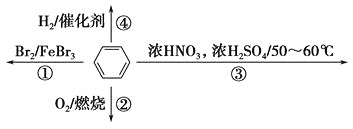
A. 反应①为取代反应,有机产物与水混合浮在上层
B. 反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C. 反应③为取代反应,有机产物是一种烃
D. 反应④中1 mol苯最多与3 mol H2发生加成反应,因为每个苯分子含有三个碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有化合物:
甲: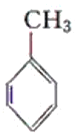 乙:
乙: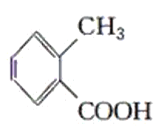 丙:
丙: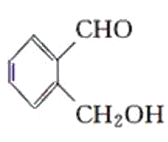
(1)请判别上述哪些化合物互为同分异构体(填序号):____________。
(2)请用一种试剂鉴别甲、乙、丙化合物。在下表中填入所选试剂及主要现象即可。________
试剂 | 现象 | |
甲 | ||
乙 | ||
丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己烯是重要的化工原料。其实验室制备流程如下:
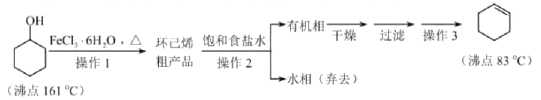
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为____________,现象为__________________。
(2)操作1![]() 装置如图所示(加热和夹持装置已略去)。
装置如图所示(加热和夹持装置已略去)。
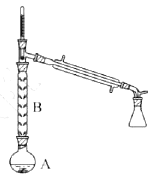
①烧瓶A中进行的可逆反应化学方程式为________________________
②仪器B的作用为____________。
(3)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,____________,弃去前馏分,收集83℃的馏分。
Ⅱ.环己烯含量的测定
在一定条件下,向![]() 环己烯样品中加入定量制得的
环己烯样品中加入定量制得的![]() ,与环己烯充分反应后,剩余的
,与环己烯充分反应后,剩余的![]() 与足量
与足量![]() 作用生成
作用生成![]() ,生成的I2用
,生成的I2用![]() 的
的![]() 标准溶液与其反应,恰好消耗
标准溶液与其反应,恰好消耗![]() 标准溶液
标准溶液![]() (以上数据均已扣除干扰因素)。
(以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:①![]()
②![]() I2+2Na2S2O3=2NaI+Na2S4O6
I2+2Na2S2O3=2NaI+Na2S4O6
(4)计算样品中环己烯的质量分数为____________(用字母表示)。
(5)下列情况会导致测定结果偏低的是____________(填序号)。
a.样品中含有苯酚杂质 b.在测定过程中部分环己烯挥发 c.![]() 标准溶液部分被氧化
标准溶液部分被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述不正确的是( )
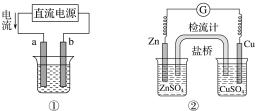
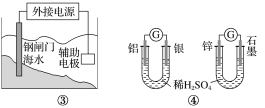
A.用图①装置实现铁上镀铜,a极为铜,电解质溶液可以是CuSO4溶液
B.图②装置盐桥中KCl的Cl-移向右烧杯
C.图③装置中钢闸门应与外接电源的负极相连获得保护
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据碘与氢气反应的热化学方程式
① I2(g)+ H2(g)![]() 2HI(g) ΔH=-9.48 kJ/mol
2HI(g) ΔH=-9.48 kJ/mol
② I2(s)+ H2(g)![]() 2HI(g) ΔH=+26.48 kJ/mol
2HI(g) ΔH=+26.48 kJ/mol
下列判断正确的是
A.254g I2(g)中通入2gH2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应②的反应物总能量比反应①的反应物总能量低
D.反应①的产物比反应②的产物稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com