
(18��)ˮ��������������Ҫ��ѧ���ʣ��й�ˮ�ķ�Ӧ�кܶࡣ
��1��ˮ���ӵĿռ乹��Ϊ___________��ˮ�����������û������������������ӣ����������ӵĵ���ʽ��___________

��2����ͼ��ijƷ�����ÿ�Ȫˮ��ǩ�IJ������ݡ������һƿ�ϸ�����ֿ�Ȫˮ����������ӵ����ʵ������ܳ���___________��
��3������½�a L��������1Lˮ�У��õ�����Һ�ܶ�Ϊb g��cm��3���û�ѧ����ʽ��ʾ��������ˮ�Լ��Ե�ԭ��___________����Һ�����ʵ���Ũ��Ϊ___________mol��L��1��
��4����֪M�������г�����һ�ֽ�������44.8 g M��ȫ���ں�ϡ�Ĺ������ᣬ��������Һ�м������������ռ���ȣ��ų�6.72 L(��״��)���塣M���ڸú�ϡ����������ӷ���ʽΪ___________________��M��ˮ�ڸ��������£�����1g��������a kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ_________________________________��
��5��ζ���dz��õĵ�ζƷ����ǰζ��������Ҫ���õ��۷��ͷ������е�һ����ʹ����ˮ��Ϊ���ǡ�
�ٵ��۷���ˮ�ⷴӦ�Ļ�ѧ����ʽ��_________________________________
��ʵ�����м������ˮ�����Ӧѡ�õ��Լ�������___________ (����ĸ)��
A��NaOH��Һ����ˮ��AgNO3��Һ B��H2SO4��Һ����ˮ��AgNO3��Һ
C��NaOH��Һ��CuSO4��Һ D��H2SO4��Һ��CuSO4��Һ
��1�����ͣ���V�͡����ͣ� ����2��1��10-4mol��
����2��1��10-4mol��
��3��NH3��H2O NH3.H2O
NH3.H2O NH4����OH����
NH4����OH���� mol/L
mol/L
��4��8Fe��30H+��3NO3��=8Fe3����3NH4����9H2O��3Fe(s)��4H2O(g)  Fe3O4(s)��4H2(g) ?H=+8aKJ/mol
Fe3O4(s)��4H2(g) ?H=+8aKJ/mol
��5���� ��A��C
��A��C
��������
�����������1����ˮ����������H��O��֮��ļ���Ϊ104.3�㣬����ˮ���ӵĿռ乹��Ϊ���ͣ���V�͡����ͣ���ˮ�����������û������������������ӣ����뷽��ʽΪH2O H++OH-������������OH-�ĵ���ʽ��
H++OH-������������OH-�ĵ���ʽ�� ����2��SO42-�����ʵ���Ϊ��19.2��10-3g/L��96g/mol=2��10-4mol/L����ƿ��Ȫˮ�������0.5L������京�е�SO42-�����ʵ��������ֵΪ2��10-4mol��0.5L=1��10-4mol����3�� ��������ˮ�Լ��Ե�ԭ���÷���ʽ��ʾΪ��NH3��H2O
����2��SO42-�����ʵ���Ϊ��19.2��10-3g/L��96g/mol=2��10-4mol/L����ƿ��Ȫˮ�������0.5L������京�е�SO42-�����ʵ��������ֵΪ2��10-4mol��0.5L=1��10-4mol����3�� ��������ˮ�Լ��Ե�ԭ���÷���ʽ��ʾΪ��NH3��H2O NH3.H2O
NH3.H2O NH4����OH��������Һ������������(a L��22.4L/mol��17g/mol)��(a L��22.4L/mol��17g/mol+1000g)��100%=17a��(17a+22400);��˸���Һ���ʵ���Ũ��Ϊ
NH4����OH��������Һ������������(a L��22.4L/mol��17g/mol)��(a L��22.4L/mol��17g/mol+1000g)��100%=17a��(17a+22400);��˸���Һ���ʵ���Ũ��Ϊ mol/L����4��n(NH3)=6.72L��22.4L/mol=0.3mol��ÿ1mol��N�ɷ�Ӧǰ��HNO3��+5�۱�Ϊ��Ӧ���-3�ۣ�����8�ۣ����Բ���0.3mol����ת�Ƶ��ӵ����ʵ���Ϊ8��0.3mol=2.4mol.�������г����Ľ�����Al��Fe�����Ƕ���+3�۵Ľ�����������������ԭ������ΪM����M��44.8=3��2.4�����M=56.��˸ý�����Fe.�����������������M���ڸú�ϡ����������ӷ���ʽΪ8Fe��30H+��3NO3��=8Fe3����3NH4����9H2O����������ɵ�Fe��ˮ������Ӧ���Ȼ�ѧ����ʽΪ3Fe(s)��4H2O(g)
mol/L����4��n(NH3)=6.72L��22.4L/mol=0.3mol��ÿ1mol��N�ɷ�Ӧǰ��HNO3��+5�۱�Ϊ��Ӧ���-3�ۣ�����8�ۣ����Բ���0.3mol����ת�Ƶ��ӵ����ʵ���Ϊ8��0.3mol=2.4mol.�������г����Ľ�����Al��Fe�����Ƕ���+3�۵Ľ�����������������ԭ������ΪM����M��44.8=3��2.4�����M=56.��˸ý�����Fe.�����������������M���ڸú�ϡ����������ӷ���ʽΪ8Fe��30H+��3NO3��=8Fe3����3NH4����9H2O����������ɵ�Fe��ˮ������Ӧ���Ȼ�ѧ����ʽΪ3Fe(s)��4H2O(g)  Fe3O4(s)��4H2(g) ?H=+8aKJ/mol����5���ٵ��۷���ˮ�ⷴӦ�Ļ�ѧ����ʽ��
Fe3O4(s)��4H2(g) ?H=+8aKJ/mol����5���ٵ��۷���ˮ�ⷴӦ�Ļ�ѧ����ʽ�� ���ڵ���ˮ��Ҫ��������·�Ӧ����������Ӧ�ü���NaOH��Һ�к����ᣬȻ����ˮ��AgNO3��ҺΪԭ����ȡ������Һ����������Һ�м�����۷�ˮ����ˮԡ���ȣ���������������֤��ˮ������������ǣ�������NaOH��Һ�кʹ������ᣬ����NaOH��Һ��CuSO4��Һ�Ƴ�����Cu(OH)2����Һ���ѵ��۵�ˮ����Һ���뵽����Cu(OH)2����Һ��������У�������ש��ɫ��������֤������ˮ��õ��������ǡ����ѡ��ΪA��C��
���ڵ���ˮ��Ҫ��������·�Ӧ����������Ӧ�ü���NaOH��Һ�к����ᣬȻ����ˮ��AgNO3��ҺΪԭ����ȡ������Һ����������Һ�м�����۷�ˮ����ˮԡ���ȣ���������������֤��ˮ������������ǣ�������NaOH��Һ�кʹ������ᣬ����NaOH��Һ��CuSO4��Һ�Ƴ�����Cu(OH)2����Һ���ѵ��۵�ˮ����Һ���뵽����Cu(OH)2����Һ��������У�������ש��ɫ��������֤������ˮ��õ��������ǡ����ѡ��ΪA��C��
���㣺�������ʵķ��ӵĿռ乹�͡�����ʽ����д����Һ�����Ӻ����IJⶨ������ʵĵ��롢���ʵ���Ũ�������������Ļ��㡢���ӷ���ʽ����ѧ����ʽ���Ȼ�ѧ����ʽ����д�������ǵļ��鷽����֪ʶ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014��������ѧ�����п��Ը߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
���Ե�ؾ��������ŵ��������ص㣬����õ��㷺Ӧ�á�п-�̼��Ե��������������ҺΪ���Һ������ܷ�ӦʽΪ��Zn��s��+2MnO2��s��+H2O��l��=Zn��OH��2��s��+Mn2O3��s����������˵����ȷ���ǣ� ��
A����ع���ʱ��MnO2������ԭ��Ӧ
B����ظ����ĵ缫��ӦʽΪ��2MnO2+H2O+2e-��Mn2O3+2OH-
C����ع���ʱ��K+����
D����ع���ʱ����·��ÿͨ��0.1mol���ӣ�п�����������ϼ���6.5g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������ѧ�����п��Ը�һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
������OH��������ͬ���������͵�����������( )
A��CH4 B��NH4+ C��Cl�� D��NH2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������У���˸����������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
(15��)ij�о�С���������װ�÷���CO��CO2�Ļ�����岢̽��CO��ԭ����ͭ�IJ���������Ƶ����ʡ���֪�Ȼ��٣�PdCl2����Һ��CO����������ɫ����(��������)���г�װ��δ������

����9ͼ��
��1���Լ�X��Y����ɫ��Ӧ���ʻ�ɫ����X��Y������ �� .
��2������װ�á����������Բ�װ��ҩƷ�رշ�Һ©��������K3����K1��K2�������CO�����۲쵽 ����ʱ���ɶ�Cװ�ý��м��Ȳ�������Ӧ����Ϊ��ɫ���塣
��3����ѯ���ϻ��������Ϣ����Cu2OΪ��ɫ���壻�ڳ����£�Cu2+����Һ���ȶ���Cu+�������������·�����Ӧ��2Cu+ =Cu2++Cu��
�ס�������ͬѧȡ������ɫ����(��M����)����ʵ�飬̽����ɷ֣�
��� | ʵ����� | ʵ����������� | �� �� |
�� | �� ��a g M�м���һ����ϡ���ᣬ��ֽ��裻 �� �����μ�ϡ����������, ��ַ�Ӧ. | �ٹ������Լ��٣� ����Ȼ��һ�������壬��Һ����ɫ | ��M��һ����Cu2O; ��M��һ����Cu. |
�� | ����ʵ���������Һ���� ������ϴ�ӡ�������� | ��������Ϊ | MΪCu��Cu2O�Ļ���� |
(i)����ͬѧ��Ϊ����ͬѧ���ý��۲��ɿ����������� .
(ii)����ͬѧ�������ͬѧ�����˼���,��Ϊ����ͬѧ�Ľ�������ȷ��,���ó�M��Cu��Cu2O�����ʵ���֮���� .
��4��Cװ�÷�Ӧ���������ӻ�������з����CO2������е���Ҫ������ .ʵ�������Dװ�ò�����ɫ���������ӷ���ʽΪ .
��5��Z�Լ�Ϊ����KI�ı���Һ����Eװ���п��ܲ����������� .
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������У���˸����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӻ�����ܹ���ָ���ķ�ɢϵ�д����������
A��c(H+)=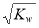 mol/L����Һ�У�NO3����NH4�� ��K+��Na+
mol/L����Һ�У�NO3����NH4�� ��K+��Na+
B����������Һ�У�HCO3����Na+��K+��CH3COO��
C������ϡ���ᷴӦ��ȡH2�����Һ�У�K+��AlO2����SO42����Br��
D�����ʵĿ�����SO2��NO��N2��NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�����и���5���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����(Salo1)��һ�������������ڷ����庬������������ģ������ͼ��ʾ(ͼ��������֮������ߴ�����ѧ�����絥����˫����)��������˵������ȷ���ǣ�
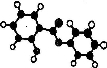
A�����ķ���ʽΪCl3Hl0O3
B��1mol������Ũ��ˮ��Ӧ����Ҫ����3mol Br2
C��1mol������ˮ�⣬��Ҫ����3mol NaOH
D������ˮ�⡢���롢�ᴿ�ɵõ������ı��Ӻ�ˮ����(���ǻ�������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������У����5�µ���������Կ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��CH4����ԭNOx�������������������Ⱦ����֪��
��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) ��H=��574 kJ/mol
��CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H=��1160 kJ/mol
��H2O(g)=H2O(l) ��H=��44kJ/mol������˵������ȷ����
A�������ʵ�����CH4�μӷ�Ӧ����Ӧ�٢�ת�Ƶĵ�������ͬ
B��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H=��530 kJ/mol
C��0.2 mol CH4��ԭNO2��N2��������H2O(g)�ų�������Ϊ164.6 kJ
D������4.48 L(��״��)CH4��ԭNO2��N2������H2O(g)������������ת�Ƶ���1.60 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������������������ѧ�ڵڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ�ˮ��Һ����ˮ��������Ե���
A��NH4Cl B��KHSO4 C��NaHCO3 D��H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����һ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪�з�Ӧ��I2��g����H2��g�� 2HI��g����H��0���÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ��x��ֵ����y��x�仯���ƺ�������
2HI��g����H��0���÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ��x��ֵ����y��x�仯���ƺ�������
ѡ�� | X | Y |
|
A | �¶� | �����ڻ��������ܶ� | |
B | I2�����ʵ��� | H2��ת���� | |
C | H2��Ũ�� | ƽ�ⳣ��K | |
D | ����Ar�����ʵ��� | �淴Ӧ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com