


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
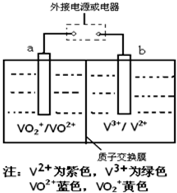 £Ø2013?Ą³ĪßŅ»Ä££©Ä³³äµēµē³ŲµÄŌĄķČēĶ¼ĖłŹ¾£¬ČÜŅŗÖŠc£ØH+£©=2.0mol?L-1£¬ŅõĄė×ÓĪŖSO42-£¬a”¢b¾łĪŖ¶čŠŌµē¼«£¬³äµēŹ±ÓŅ²ŪČÜŅŗŃÕÉ«ÓÉĀĢÉ«±äĪŖ×ĻÉ«£®ĻĀĮŠ¶Ō“Ėµē³ŲŠšŹöÕżČ·µÄŹĒ£Ø””””£©
£Ø2013?Ą³ĪßŅ»Ä££©Ä³³äµēµē³ŲµÄŌĄķČēĶ¼ĖłŹ¾£¬ČÜŅŗÖŠc£ØH+£©=2.0mol?L-1£¬ŅõĄė×ÓĪŖSO42-£¬a”¢b¾łĪŖ¶čŠŌµē¼«£¬³äµēŹ±ÓŅ²ŪČÜŅŗŃÕÉ«ÓÉĀĢÉ«±äĪŖ×ĻÉ«£®ĻĀĮŠ¶Ō“Ėµē³ŲŠšŹöÕżČ·µÄŹĒ£Ø””””£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| IO | - 3 |
| S2O | 2- 3 |
| 0.01mol?L-1KIO3 ĖįŠŌČÜŅŗ£Øŗ¬µķ·Ū£© µÄĢå»ż/mL |
0.01mol?L-Na2SO3 ČÜŅŗµÄĢå»ż/mL |
H2OµÄ Ģå»ż/mL |
ŹµŃé ĪĀ¶Č /”ę |
ČÜŅŗ³öĻÖ Ą¶É«Ź±Ėł ŠčŹ±¼ä/s | |
| ŹµŃé1 | 5 | V1 | 35 | 25 | t1 |
| ŹµŃé2 | 5 | 5 | 40 | 25 | t2 |
| ŹµŃé3 | 5 | 5 | V2 | 0 | t3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com