
| A. | 18 g H2O中所含的电子总数为10NA个 | |
| B. | 1 L 1 mol•L-1的盐酸中含有的HCl分子数为NA个 | |
| C. | 1 mol I2晶体完全升华后所得气体的体积约为22.4 L | |
| D. | 常温下78 g Na2O2中含有O2-的数目为2NA个 |
分析 A、水是10电子微粒;
B、盐酸溶液中无HCl分子;
C、碘蒸汽所处的状态不明确;
D、过氧化钠由2个钠离子和1个过氧根构成.
解答 解:A、18g水的物质的量为1mol,而水是10电子微粒,故1mol水中含10mol电子,即10NA个,故A正确;
B、HCl的水溶液为盐酸,而HCl溶于水后完全电离为氢离子和氯离子,即盐酸溶液中无HCl分子,故B错误;
C、碘蒸汽所处的状态不明确,不一定是标况,故不一定是22.4L,故C错误;
D、78g过氧化钠的物质的量为1mol,而过氧化钠由2个钠离子和1个过氧根构成,则1mol过氧化钠中含1mol过氧根,故D错误.
故选A.
点评 本题考查了物质的量的有关计算,根据物质的结构和公式来分析计算是解题关键,难度不大.


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使 pH 试纸呈红色的溶液:Fe2+、NH4+、Cl-、NO3- | |
| B. | pH=13的溶液:S2-、SO32-、SO42-、Na+ | |
| C. | 使红色石蕊试纸变蓝色的溶液:K+、HCO3-、Br-、Ba2+ | |
| D. | 含有溶质为K2SO4的溶液:AlO2-、Na+、Al3+、Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 零 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图A是实验室制取某些气体的装置.
如图A是实验室制取某些气体的装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol Al3+含有的核外电子数为3×6.02×1023 | |
| B. | 将58.5 g NaCl溶于1.00 L水中,所得NaCl溶液的浓度为1.00 mol•L-1 | |
| C. | 2 mol SO2气体与足量的O2在一定条件下反应,转移的电子数为4×6.02×1023 | |
| D. | 常温下,100mL pH=1的硫酸溶液中含有的H+离子数为0.01×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
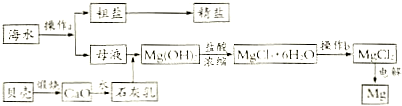
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
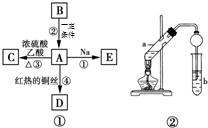 A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图①所示:
A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图①所示: CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com