
铝鞣剂[主要成分为Al(OH)2Cl]主要用于鞣制皮革.利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂的一种工艺如图:
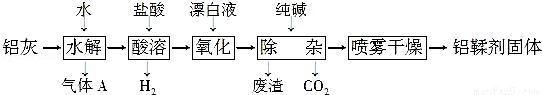
回答下列问题:
(1)气体A为 (填化学式).水解采用90℃而不在室温下进行的原因是 .
(2)酸溶时使用的酸是 (填名称).
(3)氧化时,发生反应的离子方程式为 .
(4)除杂时产生废渣的主要成分为 (填化学式),对其合理的处理方法是 .
(5)采用喷雾干燥而不用蒸发的原因是 .
(6)准确称取所制备的铝鞣剂m g,将其置于足量硝酸中,待样品完全溶解后,加入足量AgNO3溶液,充分反应,过滤、洗涤、干燥得固体ng.则样品中Al(OH)2Cl的质量分数为 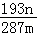 ×100% (用含m、n的代数式表示)
×100% (用含m、n的代数式表示)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年辽宁省沈阳市东北育才学校高二下期中化学试卷(解析版) 题型:选择题
某有机物结构简式为 ,下列叙述错误的是( )
,下列叙述错误的是( )
A.1 mol 该有机物在加热和催化剂作用下,最多能和4 mol H2反应
B.该有机物能使溴水褪色,也能使酸性KMnO4溶液褪色
C.该有机物遇硝酸银溶液产生白色沉淀
D.该有机物在一定条件下能发生消去反应和取代反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年全国高三模拟试卷总结化学试卷 题型:选择题
(2016春•绍兴校级期末)下列物质水溶液能导电,但该物质属于非电解质的是( )
A.Na2O B.Cl2 C.H2SO4 D.CO2
查看答案和解析>>
科目:高中化学 来源:2016届浙江省绍兴市诸暨市高考二模化学试卷(解析版) 题型:填空题
液氨和二硫化碳在一定条件下反应可以生成甲和乙两种盐.2.55g乙受热会完全分解生成等物质的量的气体丙和丁共2.24L(标况),丙能使紫色石蕊试液变蓝,另取少量FeCl3溶液,向其中滴加甲溶液,发现溶液变为血红色.请推测并回答:
(1)用离子方程式表示紫色石蕊试液变蓝原因: .
(2)写出乙受热分解的化学方程式 .
(3)甲溶液中加入足量浓NaOH溶液,加热后也能生成气体丙,写出该反应的离子方程式 .
(4)化合物甲的化学式为 .
(5)往上述血红色溶液中通入SO2,发现溶液红色褪去,请从氧化还原反应的角度解释红色褪去的原因 .
查看答案和解析>>
科目:高中化学 来源:2016届浙江省绍兴市诸暨市高考二模化学试卷(解析版) 题型:选择题
原子序数依次增大的A、B、C、D、E五种前20号的主族元素,其中A和C、B和D分别在同一主族,且它们原子的最外层电子数之和为20.已知A的氧化物能引起温室效应,E的单质能与水剧烈反应且同主族中存在金属和非金属元素,下列说法正确的是( )
A. B的氢化物的沸点比D的氢化物要高,原因是B的非金属性强
B. 比较A、C元素形成的常见氧化物,它们的化学键类型相同,晶体类型也相同
C. C的最高价氧化物的水化物酸性比D的最高价氧化物的水化物酸性强
D. 根据元素周期律,推测E在氧气中燃烧时可能生成E2O2、EO2等物质
查看答案和解析>>
科目:高中化学 来源:2016届福建省南平市浦城县高考模拟化学试卷(解析版) 题型:选择题
选项 | 实验操作 | 实验目的 |
A | 将二氧化硫气体通入紫色石蕊试液中,观察溶液颜色变化 | 证明二氧化碳具有漂白性 |
B | 向2mL1mol•L﹣1NaOH溶液中先加入3滴1mol•L﹣1FeCl3溶液,再加入3滴1mol•L﹣1MgCl2溶液 | 证明Ksp[Mg(OH)2]>ksp[Fe(OH)3] |
C | 向2mL品红溶液和2mL加入少许醋酸的品红溶液中分别滴入3滴含NaClO的“84”消毒液,观察红色褪色的快慢 | 证明随着溶液pH的减小,“84”消毒液的氧化能力增强 |
D | 相同温度下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2分解速率的影响 |
A.A B.B C.C D.D
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市青浦区高考二模化学试卷(解析版) 题型:实验题
①量取50mL 0.25mol/L硫酸倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度.
请回答:
(1)NaOH溶液稍过量的原因 .
(2)加入NaOH溶液的正确操作是 (填字母).
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(3)使硫酸与NaOH溶液混合均匀的正确操作是 .
(4)设溶液的密度均为1g/cm3,中和后溶液的比热容c=4.18J/(g•℃),请根据实验数据写出该反应的热化学方程式 .
温度 | 起始温度t1/℃ | 终止温度 | 温度差平均值(t2﹣t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 25.0 | 25.2 | 25.1 | 28.5 | 3.4 |
2 | 24.9 | 25.1 | 25.0 | 28.3 | 3.3 |
3 | 25.6 | 25.4 | 25.5 | 29.0 | 3.5 |
(5)若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量 (填“小于”、“等于”或“大于”)57.3kJ,原因是 .

查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省葫芦岛市六校协作体联考高二下期中化学试卷(解析版) 题型:选择题
氯化硼的熔点为10.7℃,在氯化硼分子中,Cl﹣B﹣Cl键角为120℃,它可以水解,水解产物之一是硼酸(H3BO3).下列有磁氯化硼的叙述正确的是( )
A.氯化硼是原子晶体
B.熔化时,氯化硼能导电
C.氯化硼分子是一种非极性分子
D.氯化硼水解得到两种弱酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高一下6月月考理科化学试卷(解析版) 题型:选择题
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌﹣锰碱性电池以氢氧化钾溶液为电解液,电池总反应Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s)下列说法中错误的是( )
A.电池工作时,锌失去电子,锌是负极
B.电池工作时,溶液中OH﹣向正极移动,K+、H+向负极移动
C.电池负极的电极反应式为:Zn﹣2e﹣+2OH﹣═Zn(OH)2
D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com