
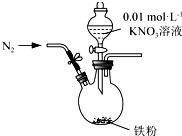
 某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应.实验过程如下:
某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应.实验过程如下:| 假设 | 实验操作 | 现象及结论 |
| 假设1:碳粉可用作还原剂,脱除硝酸盐 | 向烧杯中加入 碳粉一段时间后,测定烧杯中NO3-的浓度 | NO3-浓度无明显变化,说明假设不成立 |
| 假设2:碳粉、铁粉形成无数个微小的原电池,促进了硝酸盐的脱除 | 按下图所示组装实验装置,一段时间后,测定NO3-浓度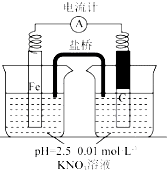 | Fe电极部分溶解,电流计指针偏转,说明假设2成立 |
分析 (1)空气中氧气会影响Fe与硝酸根离子的反应;
(2)铁粉部分溶解,溶液逐渐变为浅绿色,说明有Fe2+生成,酸性减弱Fe2+水解得到Fe(OH)2,氢氧化亚铁被氧化为氢氧化铁,颜色变为红褐色;
(3)取滤液,加入几滴K3[Fe(CN)6]溶液,有蓝色沉淀生成,注明滤液中存Fe2+;
(4)溶液中存在亚铁离子、硝酸根离子,亚铁离子含有还原性,硝酸根再酸性条件下具有氧化性,亚铁离子被氧化为铁离子;
(5)假设1:探究的是碳粉直接与NO3-反应效果,加入碳粉即可,作对照试验,溶液选取与原题中相同;
假设2:构成原电池,负极电极反应式:Fe-2e-=Fe2+,正极NO3-被还原;
③碳粉作为催化剂,提高脱除硝酸盐反应速率.
解答 解:(1)用氮气排尽装置中空气,避免空气中氧气对Fe与NO3-离子反应的干扰,
故答案为:避免空气中氧气对Fe与NO3-离子反应的干扰;
(2)铁粉部分溶解,溶液逐渐变为浅绿色,说明有Fe2+生成,待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物,酸性减弱Fe2+水解得到Fe(OH)2,白色物质为氢氧化亚铁,被氧化为氢氧化铁,颜色变为红褐色,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)用K3[Fe(CN)6]检验滤液中Fe2+的实验方案是:取滤液,加入几滴K3[Fe(CN)6]溶液,有蓝色沉淀生成,证明滤液中存Fe2+,
故答案为:取滤液,加入几滴K3[Fe(CN)6]溶液,有蓝色沉淀生成,证明滤液中存Fe2+;
(4)溶液中存在Fe2+、NO3-离子,加入硫酸,发生反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,生成的Fe3+和SCN-反应使溶液呈红色,
故答案为:溶液中存在Fe2+、NO3-离子,加入硫酸,发生反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,生成的Fe3+和SCN-反应使溶液呈红色;
(5)假设1:探究的是碳粉直接与NO3-反应效果,加入碳粉即可,作对照试验,溶液选取与原题中相同;
假设2:构成原电池,负极电极反应式:Fe-2e-=Fe2+,正极NO3-被还原,Fe电极部分溶解,电流计指针偏转等,说明假设2成立,
③碳粉作为催化剂,提高脱除硝酸盐反应速率,
故答案为:碳粉;Fe电极部分溶解,电流计指针偏转;碳粉作为催化剂,提高脱除硝酸盐反应速率.
点评 本题考查探究实验方案问题,是对学生综合能力的考查,需要学生具备扎实的基础、分析解决问题的能力,注意对基础知识的理解掌握.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点:SiO2<CO2 | B. | 沸点:H2O<H2S | ||
| C. | 晶格能:CaCl<NaCl | D. | 热稳定性:HF<HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 | 0.1MPa | 0.5MPa | 1MPa | 1.5MPa |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9988 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8520 | 0.8897 | 0.9276 | 0.9468 |
| 沸腾炉温度/℃ | 600 | 620 | 640 | 660 |
| 炉渣中CuSO4的质量分数/% | 9.3 | 9.2 | 9.0 | 8.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L1.0mo1•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 标准状况下,11.2 LNO与11.2LO2混合后所含分子数为0.75NA | |
| C. | Na2O和Na2O2混合物的物质的量为1mol,其中含有的阴离子总数为NA | |
| D. | 室温下,将9g铝片投入0.5L18.4mol•L-1的H2SO4中,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 氯气的氧化性 | 将湿润的淀粉KI试纸放于充满 Cl2的集气瓶口,试纸变蓝 |
| B | 配制 480mL 0.2mol/L NaOH溶液 | 准确称量NaOH固体4.0g溶于水,配制成 500mL溶液 |
| C | 比较 H2CO3 和 H2SO4的酸性强弱 | 室温下,用PH试纸测定浓度为O.lmol•L-1Na2CO3溶液和 0.lmol•L-1NazSO4溶液的 pH |
| D | 证明氧化性: H2O2>Fe3+ | 用硫酸酸化的H2O2滴入Fe(NO3)2洛液中,浓液变黄色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>Y | B. | 最高价含氧酸酸性:W>R | ||
| C. | 气态氢化物稳定性:Y>R | D. | 简单离子半径:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/S | 0 | 20 | 40 | 60 | 80 |
| N(NO2)/mol | 0.4 | n1 | 0.26 | n3 | n4 |
| N(N2O4)/mol | 0 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com