
长石的主要成分为硅酸盐,由前20号元素中的四种组成,化学式为XYZ3W8。其中,只有W显负价。X、Y的最外层电子数之和与Z的最高正价数相等。Y3+与W的阴离子具有相同的电子层结构。X、W的质子数之和等于Y、Z的质子数之和。下列说法错误的是( )21·cn·jy·com
A.X的离子半径>Y的离子半径
B.Z的氢化物稳定性<W的氢化物稳定性
C.Y的氧化物既能与盐酸,又能与NaOH溶液反应
D.X2W2、Y2W3两种化合物含有的化学键类型完全相同
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是
A.钠和水反应: Na+H2O=Na++OH-+H2↑
B.盐酸与氢氧化钠溶液反应: H++OH-=H2O
C.三氯化铁腐蚀印刷线路板: Fe3++Cu=Fe2++Cu2+
D.盐酸与碳酸钙反应制备二氧化碳: CO32-+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法中,正确的一组是( )
①“乙醇汽油”是在汽油里加入适量乙醇而形成的一种燃料,它是一种新型化合物
②汽油、柴油和植物油都是碳氢化合物,完全燃烧只生成CO2和H2O
③石油的分馏、裂化和煤的干馏都是化学变化
④除去乙酸乙酯中残留的乙酸,可加过量饱和碳酸钠溶液振荡后,静置分液
⑤将a g铜丝灼烧成黑色后趁热插入乙醇中,铜丝变红,再次称量铜丝的质量等于a g
⑥除去CH4中混有的少量C2H4,可将混合气体通过盛有饱和溴水的洗气瓶
A.③⑤⑥ B.④⑤⑥
C.①②⑤ D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,下列有关说法正确的是( )
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | cd | ||||||
| 3 | abef |
A.a、b两元素的单质构成原电池两极时,a一定为负极
B.e的氢化物分子和d的氢化物分子不可能含有相同的电子数
C.六种元素中,c元素与其他三种非金属元素均能形成化合物
D.c、e、f的含氧酸的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2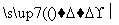 CO2+H2O。下列有关说法正确的是( )
CO2+H2O。下列有关说法正确的是( )
A.该反应为吸热反应
B.CO2分子中的化学键为非极性键
C.HCHO分子中含极性键
D.每生成1.8 g H2O消耗2.24 L O2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示方法正确的是
A.铜的原子结构示意图: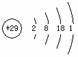 B.S2- 核外电子排布式:[Ne] 2s23p6
B.S2- 核外电子排布式:[Ne] 2s23p6
C.O原子处于基态的轨道表示式: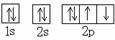
D.用电子式表示MgCl2的形成:Mg:+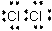 →
→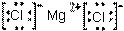
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4; ②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
A.第一电离能:③>②>① B.原子半径:③>②>①
C.电负性:③>②>① D.最高正化合价:③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
根据元素周期表和元素周期律分析下面的推断,其中错误的是
A、铍(Be)的原子失电子能力比镁弱 B、砹(At)的氢化物不稳定
C、硒(Se)化氢比硫化氢稳定 D、氢氧化锶[Sr(OH)2]比氢氧化钙的碱性强
查看答案和解析>>
科目:高中化学 来源: 题型:
硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
Ⅰ.【查阅资料】
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀盐酸。
Ⅱ.【制备产品】
实验装置如图所示(省略夹持装置):
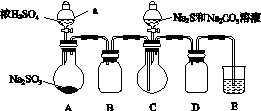
实验步骤:
(1)检查装置气密性,如图示加入试剂。
仪器a的名称是________;E中的试剂是________(选填下列字母编号)。
A.稀H2SO4
B.NaOH溶液
C.饱和NaHSO3溶液
(2)先向C中烧瓶加入Na2S和Na2CO3的混合溶液,再向A中烧瓶滴加浓H2SO4。
(3)待Na2S和Na2CO3完全消耗后,结束反应。过滤C中的混合物,滤液经________(填写操作名称)、结晶、过滤、洗涤、干燥、得到产品。
Ⅲ.【探究与反思】
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀盐酸、蒸馏水中选择)
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,____________________________________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(2)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进后的操作是______________________________________________________________________________。
(3)Na2S2O3·5H2O的溶解度随温度升高显著增大,所得产品通过________方法提纯。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com