
将体积为V mL的试管充满NO气体,按右图进行实验.当通入相同条件O2 49 mL时,液面仍在原来位置,则试管体积V为
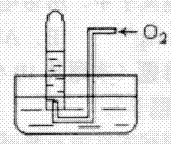 A.49mL B.30mL
A.49mL B.30mL
C.28mL D.24.5mL
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
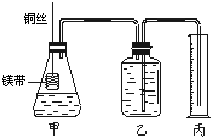 Ⅰ.铜与稀硝酸反应的离子方程式为
Ⅰ.铜与稀硝酸反应的离子方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
铁是一种历史悠久、应用最广泛、用量最大的金属。有三位同学分别用铁粉
进行如下探究实验:
甲同学用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下:

①步骤②中,除发生反应Fe+2HCl FeCl2+H2↑外,其他可能反应的离子方程式
为: 。
②可以验证溶液B中是否含有Fe2+的一种试剂是 (填选项序号)
a.稀硫酸 b.铁 c.硫氰化钾 d.酸性高锰酸钾溶液
(2)乙同学欲用少量Fe粉与足量浓硫酸反应得到硫酸亚铁。有人认为不论常温还是加热的条件下均不可行,理由是
于是乙同学将上述方案做如下改进后可获得FeSO4·7H2O,请填写下列括号中的空白:
 (3)丙同学为测试一铁片中铁元素的含量,在实验室中用m g铁片完全溶解于过量稀硫酸中,准确测定出反应生成氢气的体积为V mL (已折算成标准状况),则该铁片中铁的质量分数为(用含m、V的代数式表示) 。若排除实验仪器和操作的影响因素,试对上述方案测定结果的准确性做出判断和分析:方案 (填“准确”“不准确”“不一定准确”),理由是
(3)丙同学为测试一铁片中铁元素的含量,在实验室中用m g铁片完全溶解于过量稀硫酸中,准确测定出反应生成氢气的体积为V mL (已折算成标准状况),则该铁片中铁的质量分数为(用含m、V的代数式表示) 。若排除实验仪器和操作的影响因素,试对上述方案测定结果的准确性做出判断和分析:方案 (填“准确”“不准确”“不一定准确”),理由是
.
查看答案和解析>>
科目:高中化学 来源: 题型:
铁是一种历史悠久、应用最广泛、用量最大的金属。有三位同学分别用铁粉
进行如下探究实验:
甲同学用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下:

①步骤②中,除发生反应Fe+2HCl FeCl2+H2↑外,其他可能反应的离子方程式
为: 。
②可以验证溶液B中是否含有Fe2+的一种试剂是 (填选项序号)
a.稀硫酸 b.铁 c.硫氰化钾 d.酸性高锰酸钾溶液
(2)乙同学欲用少量Fe粉与足量浓硫酸反应得到硫酸亚铁。有人认为不论常温还是加热的条件下均不可行,理由是
于是乙同学将上述方案做如下改进后可获得FeSO4·7H2O,请填写下列括号中的空白:
 (3)丙同学为测试一铁片中铁元素的含量,在实验室中用m g铁片完全溶解于过量稀硫酸中,准确测定出反应生成氢气的体积为V mL (已折算成标准状况),则该铁片中铁的质量分数为(用含m、V的代数式表示) 。若排除实验仪器和操作的影响因素,试对上述方案测定结果的准确性做出判断和分析:方案 (填“准确”“不准确”“不一定准确”),理由是
(3)丙同学为测试一铁片中铁元素的含量,在实验室中用m g铁片完全溶解于过量稀硫酸中,准确测定出反应生成氢气的体积为V mL (已折算成标准状况),则该铁片中铁的质量分数为(用含m、V的代数式表示) 。若排除实验仪器和操作的影响因素,试对上述方案测定结果的准确性做出判断和分析:方案 (填“准确”“不准确”“不一定准确”),理由是
.
查看答案和解析>>
科目:高中化学 来源:2011-2012年呼伦贝尔市牙克石林业一中高二下学期期末考试化学试卷(带解析) 题型:实验题
(12分)欲配制一定温度下的某NaOH溶液,已知:该溶液体积为V mL,溶液密度为d g/cm3,质量分数(质量百分比浓度)为w%,物质的量浓度为c mol/L,溶液中含氢氧化钠的质量为m g. 试回答下列问题.
(1)计算:用w、d表示溶液中溶质的物质的量浓度c为________________.
(2)某学生用托盘天平称量小烧杯的质量(烧杯中盛NaOH),称量前把游码放在标尺的零刻度,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将________________(填“高于”或“低于”)右边的托盘,欲使天平平衡,所进行的操作为____________ ________________ ,假定最终称量小烧杯的质量为________________(填“32.6 g”或“32.61 g”).
(3)在标尺(图)上画出游码位置(画“△”表示).
(4)定容后将溶液振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线,则测得溶液的物质的量浓度将__________________(填“偏大”、“偏小”或“无影响”).
查看答案和解析>>
科目:高中化学 来源:2011-2012年呼伦贝尔市高二下学期期末考试化学试卷(解析版) 题型:实验题
(12分)欲配制一定温度下的某NaOH溶液,已知:该溶液体积为V mL,溶液密度为d g/cm3,质量分数(质量百分比浓度)为w%,物质的量浓度为c mol/L,溶液中含氢氧化钠的质量为m g. 试回答下列问题.
(1)计算:用w、d表示溶液中溶质的物质的量浓度c为________________.
(2)某学生用托盘天平称量小烧杯的质量(烧杯中盛NaOH),称量前把游码放在标尺的零刻度,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将________________(填“高于”或“低于”)右边的托盘,欲使天平平衡,所进行的操作为____________ ________________ ,假定最终称量小烧杯的质量为________________(填“32.6 g”或“32.61 g”).
(3)在标尺(图)上画出游码位置(画“△”表示).

(4)定容后将溶液振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线,则测得溶液的物质的量浓度将__________________(填“偏大”、“偏小”或“无影响”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com