
有一块铝铁合金溶于足量的盐酸中,再用过量的氢氧化钠溶液处理,将产生的沉淀过滤,洗涤、干燥、灼烧,完全变成红色粉末,经称量红色粉末和合金的重量恰好相等,
则合金中铝的质量分数为:
A.30% B.47.6% C.52.4% D.70%
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源:2016-2017学年安徽省六安市高一下学期第一次阶段检测化学试卷(解析版) 题型:选择题
对某酸性溶液(可能含有Br-、SO42-、H2SO3、NH4+)分别进行如下实验:①加热时放出的气体可以使品红溶液褪色;②加碱调至碱性后,加热时放出的气体可以使湿润的红色石蕊试纸变蓝;⑨加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸。对于下列物质不能确认其在溶液中是否存在的是( )
A.Br- B.SO42- C.H2SO3 D.NH4+
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(一)化学试卷(解析版) 题型:填空题
氢氧化镁是已知用途广泛、极具开发前景的环保材料,广泛应用在阻燃、废水中和、烟气脱硫等方面。镁硅酸盐矿石[主要成分Mg3Si2O5(OH)4,含氧化铝、氧化铁、氧化亚铁等杂质]可用于生产氢氧化镁,简要工艺流程如下:

已知:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)对矿石焙烧的目的是_______________________。
(2)加入H2O2溶液反应的离子方程式是___________________。
(3)向溶液Ⅰ中加入的X可以是______________,作用是______________。
(4)加入氨水时,Mg2+转化率随温度t的变化如图所示:

①溶液Ⅱ中发生反应的离子方程式是__________________。
②t1前Mg2+转化率增大的原因是__________________;t1后Mg2+转化率下降的原因是(用化学方程式表示)______________。
查看答案和解析>>
科目:高中化学 来源:2017届北京市朝阳区高三第一次(3月)综合练习理综化学试卷(解析版) 题型:选择题
某学生探究0.25mol/L Al2( SO4)3溶液与0.5mol/L Na2CO3溶液的反应,实验如下:
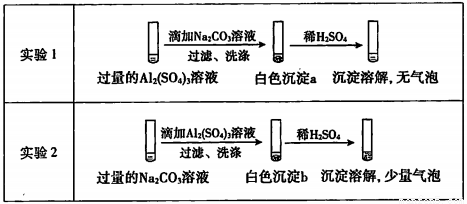
下列分析不正确的是
A. 实验I中,白色沉淀a是Al(OH)3
B. 实验2中,白色沉淀b含有CO32-
C. 实验l、2中,白色沉淀成分不同的原因与混合后溶液的pH无关
D. 检验白色沉淀a、b足否洗涤干净,均可用盐酸酸化的BaCl2溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一下学期第一次月考(3月)化学试卷(解析版) 题型:计算题
将0.1 mol的镁、铝混合物溶于100 mL 2mol/L H2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。

当V1=160mL时,则金属粉末中n(Mg)=________ mol,V2=_____________mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH) _____________mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:_____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一下学期第一次月考(3月)化学试卷(解析版) 题型:选择题
同一周期的X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性顺序为HXO4>H2YO4>H3ZO4,则下列判断错误的是
A. 原子半径:X>Y>Z B. 气态氢化物的稳定性:HX>H2Y>ZH3
C. 元素原子得电子能力:X>Y>Z D. 阴离子的还原性:Z3->Y2->X-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一下学期第一次月考(3月)化学试卷(解析版) 题型:选择题
下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )

A. 原子半径:Z>Y>X
B. 气态氢化物的稳定性:W>R
C. W最高价氧化物对应的水化物是强碱
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源:四川省成都市北湖校区2016-2017学年高一3月月考化学试卷 题型:选择题
右图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是( )

A. X与M形成的一个阴离子中含有29个电子
B. 气态氢化物沸点Y>R
C. 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D. Z单质能从M与R元素构成的盐溶液中置换出单质M
查看答案和解析>>
科目:高中化学 来源:2017届高考信息卷(全国卷I)理科综合(一)化学试卷(解析版) 题型:填空题
甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度 | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.00 | 2.5 |
③3H2(g)+CO2(g) | K3 | ||
(1)在体积一定的密闭容器中发生反应②,达到平衡后升高温度,下列说法正确的是____________
A.平衡正向移动 B.达到新的平衡后体系的压强增大
C.H2的转化率增大 D.体系的密度增大
(2)某温度下反应①中H2的平衡转化率(α)与体系总压强(p)的关系如图所示,若开始加入2molH2和1molCO,A点时容器的体积为1L,则B点的化学平衡常数为_______。

(3)据反应①与②可推导出Kl、K2与K3之间的关系,则K3=__________。(用K1、K2表示)。500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g) 的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时v正_______ v逆(填“> ”、“= ”或“< ")。
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)一反应时间t变化曲线l如图所示,若在t0时刻分别改变一个条件,曲线I变为曲线II和曲线III。

当曲线I变为曲线II时,改变的条件可能是________。当曲线I变为曲线III时,改变的条件可能是___________。
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与bmol/LBa (OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com