
某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数为5.1%,300mL该溶液中氯离子的物质的量为
| A.0.37mol | B.0.63mol | C.0.74mol | D.1.5mol |
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:单选题
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.常温常压下,22.4 L乙烯中C-H键数为4NA |
| B.1 mol甲醇中含有C-H键的数目为4NA |
| C.常温常压下,7.0 g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| D.17 g羟基(-OH)所含有的电子数为7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A.28g氮气所含有的原子数目为NA |
| B.化学反应中1mol金属镁变成镁离子时失去电子数目为2NA |
| C.标准状况下,22.4L水中含有NA个水分子 |
| D.标准状况下,22.4L氯化氢所含的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某溶液中只含有Na+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为
| A.1∶2 | B.1∶4 | C.3∶4 | D.3∶2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列化学用语正确的是
A.中子数为20的氯原子: |
| B.硫酸的电离方程式:H2SO4=H2++SO42— |
| C.漂白粉的有效成分:CaCl2 |
| D.明矾的化学式:KAl(SO4)2?12H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设阿伏加德罗常数为NA, 下列叙述中正确的是
| A.常温常压下, 32克氧气中原子个数为NA |
| B.标准状况下, 1mol H2O的体积为22.4L |
| C.常温常压下, 1molH2的质量为2克 |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有的Cl-数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.铁与足量稀硝酸反应,1mo1Fe失去电子数为3nA |
| B.常温常压下,22.4L乙烯中含极性共价键数目为5nA |
| C.1L1mol?L—1的NH4Cl溶液中有nA个NH4+ |
| D.1mol冰醋酸和lmo1乙醇在浓硫酸加热下充分反应生成H2O个数为nA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
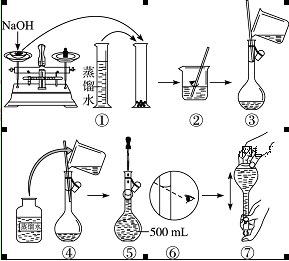
配制400 mL 0.5 mol·L-1的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为______。
(2)某学生用托盘天平称量一个小烧杯的质量,称量前把游码放在标尺的零刻度处,天平静止时发现 指针在分度盘的偏右位置,此时左边的托盘将______(填“高于”或“低于”)右边的托盘。欲使天平平衡,所进行的操作为_______。假定最终称得小烧杯的质量为______(填“32.6 g”或“31.61 g”),
(3)配制方法:设计五个操作步骤:
① 向盛有NaOH的烧杯中加入200 mL蒸馏水使其溶解,并冷却至室温;
② 继续往容量瓶中加蒸馏水至液面接近刻度线1~2 cm处;
③ 将NaOH溶液沿玻璃棒注入500 mL容量瓶中;
④ 在烧杯中加入少量的蒸馏水,小心洗涤2~3次后移入容量瓶;
⑤ 改用胶头滴管加蒸馏水至刻度线,加盖摇匀。
试将以上操作排出先后顺序______。
(4)某学生实际配制NaOH溶液的浓度为0.48 mol·L-1,原因可能是______。
| A.使用滤纸称量氢氧化钠固体 |
| B.容量瓶中原来存有少量蒸馏水 |
| C.溶解NaOH的烧杯未经多次洗涤 |
| D.胶头滴管加水后定容时仰视刻度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com