
| A. | c(H+) | B. | c(X-) | C. | $\frac{c({H}^{+})}{c(HX)}$ | D. | $\frac{c(HX)}{c({H}^{+})}$ |
分析 HX是弱电解质,加水稀释促进电离,但HX电离增大程度小于溶液体积增大程度,则溶液中c(X-)、c(H+)的浓度都减小;稀释后溶液中氢离子的物质的量增大,HX的物质的量减小,据此判断二者浓度之比的变化.
解答 解:用水稀释0.1mol/L一元弱酸HX时,溶液中随着水量的增加,HX的电离程度逐渐增大,则溶液中n(X-)、n(H+)增大,由于溶液体积增大的幅度大于n(X-)、n(H+)增大幅度,所以溶液中c(X-)、c(H+)都减小,故A、B错误;
稀释后溶液中n(X-)、n(H+)增大,溶液的体积相同,则$\frac{c({H}^{+})}{c(HX)}$的比值增大,故C正确、D错误,
故选C.
点评 本题考查弱电解质电离,题目难度中等,明确弱电解质电离特点是解本题关键,注意:加水稀释虽然增大醋酸电离程度,但溶液中氢离子浓度减小而不是增大,为易错点.


 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤矸石中的金属氧化物均溶于水,且都能与水反应 | |
| B. | 煤矸石含有的酸性氧化物对应的水化物中,酸性最强的是H3PO4 | |
| C. | 煤矸石可用于生产矸石水泥、耐火砖等建筑材料 | |
| D. | 用盐酸可以溶解煤矸石中的所有氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| B. | 手机上用的锂离子电池属于二次电池 | |
| C. | 燃料电池能把化学能转化成电能 | |
| D. | 已知反应2CO(g)=2C(s)+O2(g)的△H>0、△S<0,那么高温下可自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量是一个物理量,物质的量的单位是摩尔 | |
| B. | 2 mol水的摩尔质量是1 mol水的摩尔质量的2倍 | |
| C. | N2、CO组成的混合气体28g,其物质的量为1mol | |
| D. | 标准状况下,2L二氧化碳和3L一氧化碳所含有的原子数目相等. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
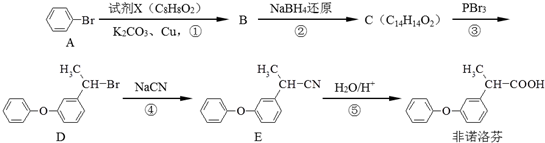
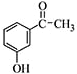 ;C:
;C: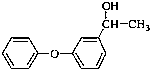 .
.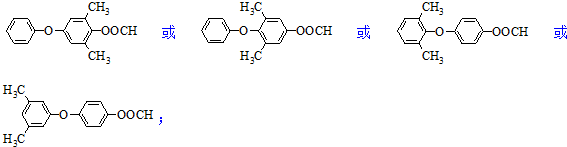 .
.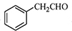 为原料制备
为原料制备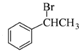 的合成路线流程图如下:
的合成路线流程图如下:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com