
| A、氨气通过无水氯化钙粉末 |
| B、氢气通过灼热的氧化铜粉末 |
| C、铝与氧化铁发生铝热反应 |
| D、将锌粒投入到硝酸铜溶液中 |


科目:高中化学 来源: 题型:
| A、制作航天服的聚酯纤维和用于制光缆的光导纤维都是新型无机非金属材料 |
| B、使用太阳能、风能等清洁能源能减少PM2.5的污染 |
| C、水泥、玻璃、水晶饰物都是硅酸盐制品 |
| D、用浸泡过溴的四氯化碳溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2012 年环保热词“PM2.5”是指大气中直径小于或等于2.5 微米(1 微米=1×10-6 米)的颗粒,“PM2.5”与空气形成的分散系属于胶体 |
| B、石墨烯是一种从石墨材料中用“撕裂”方法剥离出的单层碳原子面材料,用这种方法从C60、金刚石等中获得“只有一层碳原子厚的碳薄片”也必将成为研究方向 |
| C、任何元素的原子都是由核外电子和核内中子、质子组成的 |
| D、分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入适量的氯化铵晶体后,两溶液的pH均碱小 |
| B、温度下降10°C,两溶液的pH均不变 |
| C、分别加水稀释10倍,两溶液的pH仍相等 |
| D、用同浓度的盐酸中和,消耗盐酸的体积相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同一主族的金属元素,从上到下阳离子的氧化性逐渐增强 |
| B、最外层电子数相同的微粒,其化学性质一定相似 |
| C、同周期金属元素的氧化物对应水化物的碱性从左到右依次增强 |
| D、第ⅦA族元素从上到下,其氢化物稳定性减弱而还原性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
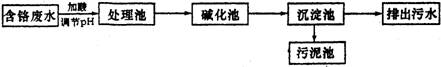
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向稀硝酸中加入铁粉 |
| B、向氯化铝溶液中加入过量的氨水 |
| C、向NaOH溶液中通入CO2气体 |
| D、向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com