
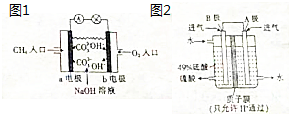
 碳和硫的化合物在生产和生活中的应用非常广泛,清洁能源的开发、煤的综合利用等是实验“低碳生活”、减少空气污染的重要途径,试运用所学知识,回答下列问题:
碳和硫的化合物在生产和生活中的应用非常广泛,清洁能源的开发、煤的综合利用等是实验“低碳生活”、减少空气污染的重要途径,试运用所学知识,回答下列问题:分析 (1)燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,此时生成的水必须为液态,利用盖斯定律来分析;化学反应的实质是旧键的断裂和新键的生成;
(2)①燃料电池中,通入燃料的电极是负极,;
②根据电池反应式确定溶液pH变化.
(3)本题为SO2与O2反应生成SO3,SO3再与水化合生成硫酸,根据硫酸的出口判断正负极,负极发生氧化反应,正极发生还原反应,原电池放电时,电解质溶液中阳离子向正极移动.
解答 解:(1)燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,此时生成的水必须为液态,已知:
①2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H1=-1214kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566kJ•mol-1
根据盖斯定律,将$\frac{①+②}{2}$可得:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=$\frac{(-1214KJ/mol)+(-566KJ/mol)}{2}$=-890KJ/mol,即甲烷的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890KJ/mol;
化学反应的实质是旧键的断裂和新键的生成,旧键的断裂吸收能量,新键的形成放出能量,反应放热是因为形成新键时放出的能量大于断裂旧键时吸收的能量,故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890KJ/mol;反应中形成新键时放出的能量大于断裂旧键时吸收的能量;
(2)①燃料电池中,通入燃料的电极是负极,故答案为:a;
②在碱性溶液中,甲烷燃料电池的总反应式为CH4+2O2+2OH-=CO32-+3H2O,溶液中氢氧根离子被消耗,导致溶液的pH减小,故答案为:减小.
(3)该原电池中,负极上失电子被氧化,所以负极上投放的气体是二氧化硫,二氧化硫失电子和水反应生成硫酸根离子和氢离子,正极上投放的气体是氧气,正极上氧气得电子和氢离子反应生成水,根据硫酸和水的出口方向知,B极是负极,A极是正极,所以B极上的电极反应式为:SO2-2e-+2H2O═SO42-+4H+,
故答案为:SO2-2e-+2H2O═SO42-+4H+;
点评 本题考查热化学反应方程式的书写、原电池原理,注意原电池放电时,电解质溶液pH的变化情况,为易错点.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaCl、NaBr、NaI混合溶液中通入F2:I-、Br-、Cl- | |
| B. | 向NaCl、NaI、Na2S混合溶液中滴加AgNO3溶液:S2-、I-、Cl- | |
| C. | 向FeCl3、CuCl2、HCl混合溶液中加入Zn粉:Cu2+、Fe3+、H+ | |
| D. | 向NaAlO2、Na2CO2、NaOH混合溶液中滴加稀盐酸:AlO2-、CO32-、HCO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4(熔融)═Na++H++SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | CH3COOH?CH3COO-+H+ | D. | H2CO3?2H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com