
【题目】Ⅰ.在锌与某浓度的盐酸反应的实验中,实验员得到下面的结果:
锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸花的时间(s) | |
A | 2 | 薄片 | 5 | 400 |
B | 2 | 薄片 | 15 | 200 |
C | 2 | 薄片 | 25 | 100 |
D | 2 | 薄片 | 35 | 50 |
E | 2 | 薄片 | 45 | 25 |
F | 2 | 粉末 | 15 | 5 |
(1)写出实验中发生反应的离子方程式:___________,该反应是_____反应(填“放热”或“吸热”);
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花____ s。
(3)对比结果B与F,解释结果F那么快的原因:________
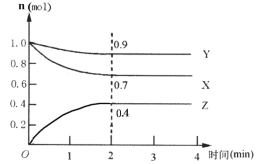
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0~4分钟各物质的量的变化情况如图所示(X、Y、Z均为气体)。
(1)该反应的的化学方程式为_______;
(2)反应开始至2分钟时,X的平均反应速率为______;
(3)能说明该反应已达到平衡状态的是______;
a.每消耗3molX,同时消耗1molY
b.容器内压强保持不变
c.Z的浓度不再变化
d.容器内混合气体的密度保持不变
(4)由下图求得平衡时Y的转化率为_____。
【答案】Ⅰ(1)Zn+2H+=Zn2++H2↑放热(2)12.5(3)B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要比块状时的接触面大得多Ⅱ(1)3X+Y![]() 4Z(2)0.03mol/(L·min)(3)c(4)10%
4Z(2)0.03mol/(L·min)(3)c(4)10%
【解析】
试题Ⅰ(1)锌是活泼金属,锌与盐酸反应生成ZnCl2和氢气,则反应的离子方程式为Zn+2H+ =Zn2++ H2↑;活泼金属与酸的反应是放热反应。
(2)通过观察A—F的实验数据对比可知,温度每升高10℃,反应速率增大到原来的2倍,根据表格E中数据可知,2g锌薄片溶解于45℃的酸中花的时间为25s,则在55℃时反应速率是45℃时的2倍,花的时间为12.5s。
(3) 对比结果B与F,速率与Zn的状态有关,B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要比块状时的接触面大得多,所以结果F那么快。
Ⅱ(1)由图象可以看出,X、Y的物质的量逐渐减小,X、Y为反应物,Z的物质的量逐渐增多,所以Z为生成物,当反应到达2min时,△n(X)=0.3mol,△n(Y)=0.1mol,△n(Z)=0.4mol,化学反应中,各物质的物质的量的变化值与化学计量数呈正比,则△n(A):△n(B):△n(C)=3:1:4,所以反应的化学方程式为3X + Y![]() 4Z。
4Z。
(2)由图象可以看出,反应开始至2分钟时,△n(X)=0.3mol,X的平均反应速率为0.3mol÷(5L×2min) =0.03mol/(L.min)。
(3)a.每消耗3molX,同时消耗1molY,表达的都是正反应速率,无法判断反应是否达到平衡,a项错误;b. 该反应为前后气体体积不变的反应,压强始终保持不变,不能作为判断反应是否达到平衡的标志,b项错误;c.Z的浓度不再变化,说明反应达到平衡状态,c项正确;d. 该反应在5L恒容容器中进行,所有物质又都是气体,所以反应体系的密度始终不变,不能作为平衡状态的判断标志,d项错误;答案选c。
(4)由图可知:达平衡时,△n(Y)=0.1mol,所以Y的转化率为0.1mol÷1mol×100%=10%。


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】控制适合的条件,将反应Fe3++AgFe2++Ag+设计成如下图所示的原电池(盐桥装有琼脂-硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知接通后,观察到电流计指针向右偏转。下列判断不正确的是( )。
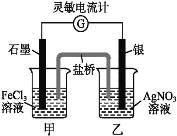
A. 在外电路中,电子从银电极流向石墨电极
B. 盐桥中的K+移向甲烧杯
C. 电流计指针居中后,往甲烧杯中加入一定量的铁粉,电流计指针将向左偏转
D. 一段时间后,电流计指针反向偏转,越过0刻度,向左边偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质反应后,再滴入KSCN溶液,显红色的是( )
A.过量铁与稀盐酸B.过量氯水与FeCl2溶液
C.过量铁粉与CuCl2溶液D.过量铁粉与FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X和Y可以形成XY4型化合物,若X的原子序数为a,Y的原子序数为b,则a和b的相互关系不可能是( )
A. a-13 = b
B. a +8 = b
C. b-11 = a
D. b+5 = a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】软锰矿(主要成分为MnO2)可用于制备锰及其化合物,现代冶炼金属锰的工艺流程如下图所示,步骤中杂质离子逐一沉淀。

下表为t℃时,有关物质的Ksp
物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
Ksp | 4.0×10-38 | 2.2 | 5.5 | 1.9 | 6.3 | 9.1 | 2.5 | 2.2 |
软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4===12MnSO4+6CO2↑+18H2O
(1)写出一种能提高还原浸出速率的措施:_________________________
(2)调节pH 步骤中生成的沉淀为________。加入MnF2的主要目的是除去__________ (填“Ca2+”、“Fe3+”或“Cu2+”)
(3)等浓度的(NH4)2S与(N4)2SO4 溶液中,NH4+的浓度大小为:前者________后者(填“>”、“< ” “=” )。
(4)由MnSO4制取MnCO3往MnSO4溶液中加入(NH4)2CO3溶液生成MnCO3,同时还会产生Mn(OH)2,可能的原因有:MnCO3(s)+2OH-(aq)![]() Mn(OH)2(s)+CO
Mn(OH)2(s)+CO![]() (aq),t℃时,计算该反应的平衡常数K=_________________(保留一位小数)。
(aq),t℃时,计算该反应的平衡常数K=_________________(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO3·3H2O。实验过程如下:

(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)===Mg2+(aq)+CO2(g)+H2O(l) ΔH=-50.4 kJ·mol–1
Mg2SiO4(s)+4H+(aq)="==2" Mg2+(aq)+H2SiO3(s)+H2O(l) ΔH=-225.4 kJ·mol–1
酸溶需加热的目的是_____ _;所加H2SO4不宜过量太多的原因是____ __。
(2)加入H2O2氧化时发生发应的离子方程式为__________
(3)用如图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。

①实验装置图中仪器A的名称为__________。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂, 、静置、分液,并重复多次。
(4)请补充完整由萃取后得到的水溶液制备MgCO3·3H2O的实验方案:边搅拌边向溶液中滴加氨水, ,过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO3·3H2O。
[已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖类的叙述正确的是( )
A.含有C、H、O三种元素的有机物叫糖类
B.糖类物质均能与银氨溶液在加热时发生反应生成银镜
C.糖类物质都有甜味
D.糖类物质是绿色植物光合作用的产物,是动植物所需能量的重要来源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应生成CO2的量与反应时间的关系如图所示。下列结论不正确的是
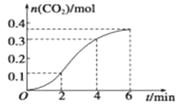
A. 反应在2~4 min内平均反应速率最大
B. 反应开始4 min内温度比浓度对反应速率的影响大
C. 4 min后,反应速率减小的主要原因是c(H+)减小
D. 反应在2~4 min内生成CO2的平均反应速率为v(CO2)=0.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:[CoCl4]2-(蓝色)与[Co(H2O)6]2+(粉红色)之间存在如下平衡:[CoCl4]2-+6H2O [Co(H2O)6]2++4Cl- △H<0。现有呈现紫色的氯化钴溶液。
(1)甲同学向上述溶液中通入HC1,发现溶液变为___色;
(2)乙同学向上述溶液中加水,平衡___(填“向右”、“向左”或“不”)移动。为使平衡保持该移动方向,还可采取的措施有____(写一种)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com