
【题目】下列关于有机化合物的说法正确的是( )
A.乙醇和乙酸中都存在碳氧双键
B.甲烷和乙烯都可以与氯气反应
C.高锰酸钾可以氧化苯和甲烷
D.乙烯可以与氧气发生加成反应,苯不能与氢气加成
科目:高中化学 来源: 题型:
【题目】高温下用H2还原CuCl制备活性铜,反应原理如下:
2Cu(s)+Cl2(g) ![]() 2CuCl(s) ΔH1=-36 kJ·mol-1①
2CuCl(s) ΔH1=-36 kJ·mol-1①
H2(g)+2CuCl(s) ![]() 2Cu(s)+2HCl(g) ΔH2②
2Cu(s)+2HCl(g) ΔH2②
有关物质的键能数据如下表:
物质 | H2 | Cl2 | HCl |
键能/kJ·mol-1 | 436 | 243 | 432 |
(1)ΔH2=________kJ·mol-1。
(2)经测定反应②制备活性铜的反应趋势大,原因是__________。
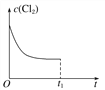
(3)在某温度下,反应①达到平衡状态,在tl时,增加压强到原来的2倍(Cu的量足够),在图中画出Cl2浓度的变化趋势线。________________________
(4)白色不溶于水的CuCl可以由电解法制得,如图所示:
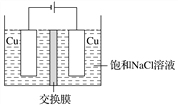
①装置中用的交换膜为________。
A.阳离子交换膜 B.阴离子交换膜
C.质子交换膜 D.氢氧根离子交换膜
②阳极的电极反应式为______________________________________________。
(5)已知CuCl可溶解于稀硝酸,写出该反应的化学方程式:
________________________________________________________________________。
(6)根据已学知识写出制取CuCl的一种方法,用化学方程式表示:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钒(V)广泛应用于航空、化工、能源等行业。
(1)钒元素基态原子的电子排布式为__________,3d 能级上的未成对电子数为___________。
(2)VCl2溶液与乙二胺(H2N—CH2—CH3—NH4 )可形成配离子[V(En)2]2+ (En是乙二胺的简写),该配离子中所含非金属元素的电负性由大到小的顺序是___________ (用元素符号表示)。乙二胺分子中氮原子的杂化轨道类型为_____________,乙二胺和三甲胺[N(CH3)3]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是______________。
(3)LiVH4是一种特殊的还原剂,可将乙酸直接还原成乙醇。CH3COOH和CH3CH2OH分子中σ键数目之比为 ____________。
(4)钒能形成多种配合物,钒的两种配合物 X、Y的化学式均为 V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来)。
X | X | Y | Y | |
试剂 | BaCl2溶液 | AgNO3溶液 | BaCl2溶液 | AgNO3溶液 |
现象 | 白色沉淀 | 无明显变化 | 无明显变化 | 白色沉淀 |
则 X的配离子为___________,Y的配体是 __________。
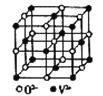
(5)VO晶体的晶胞结构如图所示,VO晶体中 V2+的配位数为 __________________。若该晶胞边长为 b nm,则该晶体的密度为__________ (用含 b,NA的代数式表示)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,将 1.0 L wmoI/L CH3COOH 溶液与 0.1 mol NaOH固体混合,充分反应。然后向混合液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。 下列叙述正确的是
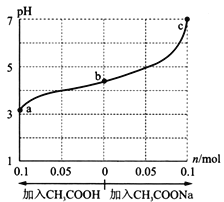
A. a、b、c对应的混合液中,水的电离程度由大到小的顺序是c>a>b
B. b点混合液中 c(Na+) >c(CH3COO-)
C. 加入CH3COOH过程中,![]() 增大
增大
D. 25℃时,CH3COOH的电离平衡常数Ka=![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯和其他无机原料合成环状酯E和高分子化合物H的示意图如下所示:
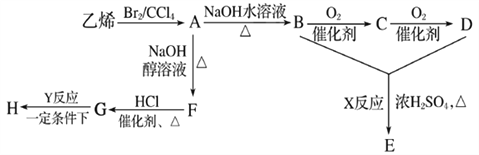
请回答下列问题:
(1)写出以下物质的结构简式:A___________,F___________,C___________。
(2)写出以下反应的反应类型:X_________________,Y__________________。
(3)写出以下反应的化学方程式:A→B:_______________;G→H:___________。
(4)若环状酯E与NaOH水溶液共热,则发生反应的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:电池的理论比能量指单位质量的电极材料理论上能释放出的最大电能。镁一空气电池的总反应方程式为:2Mg+O2+2H2O=2Mg(OH)2,其工作原理如下图所示,下列说法不正确是

A. 该电池的放电过程的正极反应为O2+4e-+2H2O=4OH-
B. 为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
C. 与铝一空气电池相比,镁一空气电池的比能量更高
D. 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为基本原料可制备许多物质,如:
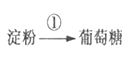

下列有关说法中正确的是( )
A. 淀粉是糖类物质,有甜味,与纤维素互为同分异构体
B. 反应③是消去反应,反应④是加聚反应,反应⑤是氧化反应
C. 乙烯、聚乙烯分子中均含有碳碳双键,均可被酸性KMnO4溶液氧化
D. 反应②是葡萄糖发生水解生成了CH3CH2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com