
浙江省从2013年12月1日零时起,车用汽油升级为“国Ⅳ”标准,汽油中的硫含量下降三分之二,对二氧化硫的排放有了大大的改善,SO2可以用Fe(NO3)3溶液吸收,某化学兴趣小组对SO2和Fe(NO3)3溶液的反应 [0.1 mol·L-1的Fe(NO3)3溶液的pH=2]做了相应探究。
探究Ⅰ:
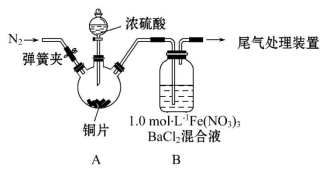
(1)某同学进行了下列实验:取12.8 g铜片和20 mL 18 mol·L-1的浓硫酸放在三颈瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余,同时根据所学的知识同学们认为还有较多的硫酸剩余。
①配制1.0 mol·L-1的Fe(NO3)3溶液,需准确称量一定质量的Fe(NO3)3固体,在烧杯中溶解恢复到室温后,将溶液转移到容量瓶中,再经过洗涤、定容、摇匀可配得溶液,请回答将溶液转移至容量瓶中的操作方法_______________________ 。
②该同学设计求反应后余酸的物质的量的实验方案是测定产生气体的量。其方法有多种,请问下列方案中不可行的是 (填字母)。
A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称重
B.将产生的气体缓缓通入足量Na2S溶液后,测量所得沉淀的质量
C.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况)
探究Ⅱ:
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是 。
(3)装置B中产生了白色沉淀,分析B中产生白色沉淀的原因,提出下列三种猜想:
猜想1:SO2与Fe3+反应;
猜想2:在酸性条件下SO2与 NO3-反应;
猜想3: 猜想3: SO2在酸性条件下都与Fe3+、 NO3-反应;
①按猜想1,装置B中反应的离子方程式是 。
证明该猜想1中生成的还原产物,某同学取少量溶液滴加几滴酸性高锰酸钾溶液,紫红色褪去,请分析该同学做法是否正确 (填“正确”或“不正确”),理由是 。
②按猜想2,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列某种溶液,在相同条件下进行实验。应选择的替换溶液是 (填序号)。
a.1.0 mol·L-1稀硝酸
b.pH=1的FeCl3溶液
c.6.0 mol·L-1NaNO3和0.2 mol·L-1盐酸等体积混合的溶液
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
某一有机物A可发生下列变化:已知C为羧酸,且C、E不发生银镜反应,则A的可能结构有

A.4种 B.3种 C.2种 D.1种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一下期中化学试卷(解析版) 题型:推断题
以石油裂解气为原料,通过一系列化学反应可得到重要的化工产品增塑剂G。

请回答下列问题:
(1)反应①化学方程式为 。
(2)反应②③的目的是: 。
(3)写出反应③的化学方程式: 。写出反应⑥的化学方程式: 。
(4)写出B的结构简式 。B被氧化成C的过程中会有中间产物生成,该中间产物可能是 (写出一种物质的结构简式),检验该物质存在的试剂是__________。
(5)写出生成G的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一下期中化学试卷(解析版) 题型:选择题
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属于离子型碳化物。请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是( )
A.ZnC2水解生成乙烷(C2H6) B.Al4C3水解生成丙炔(C3H4)
C.Mg2C3水解生成丙炔(C3H4) D.Li2C2水解生成乙烯(C2H4)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
为了研究在温度对苯催化加氢的影响,以检验新型镍催化剂的性能。采用相同的微型反应装置,压强为0.78Mpa,氢气、苯的物质的量之比为6.5:1。定时取样分离出氢气后,分析成分得如下表结果:
温度/℃ | 85 | 95 | 100 | 110~240 | 280 | 300 | 340 | |
质量分数(%) | 苯 | 96.05 | 91.55 | 80.85 | 0 | 23.35 | 36.90 | 72.37 |
环己烷 | 3.95 | 8.45 | 19.15 | 100 | 76.65 | 63.10 | 27.63 | |
下列说法错误的是 ( )
A.当温度超过280℃,苯的转化率迅速下降,可能是因为该反应为吸热的可逆反应
B.在110~240℃苯的转化率为100%。说明该镍催化剂活性较高,能够在较宽的温度范围内催化而且不发生副反应
C.增大压强与提高氢气、苯的物质的量比都有利于提高苯的转化率
D.由表中数据来看,随着反应温度的升高,苯的转化率先升高后降低
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
下列有关用水杨酸和乙酸酐制备阿司匹林(乙酰水杨酸)的说法中正确的是 ( )
A.为控制水浴温度为85~90℃,把温度计插入反应液中
B.为除去阿司匹林中混有的杂质,可在粗产品中加足量NaHCO3溶液、搅拌、过滤、洗涤沉淀,干燥即得精品
C.一定条件下,1mol阿司匹林最多可与2mol的NaOH反应
D.可用FeCl3溶液检验阿司匹林中是否含有未反应完的水杨酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高一实验班下期中化学试卷(解析版) 题型:实验题
某学习小组探究金属与不同酸反应的差异,以及影响反应速率的因素。
实验药品:2.0moL/L盐酸、4.0mol/L盐酸、2 .0mol/L硫酸、4.0mol/L硫酸,相同大小的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50. 0mL,金属用量均为9.0g。
0mL,金属用量均为9.0g。
(1)帮助该组同学完成以上实验设计表。
实验目的 | 实验 编号 | 温度 | 金属铝 形态 | 酸及浓度 |
1.实验①和②探究盐酸浓度对该反应速率的影响 2.实验②和③探究 3.实验②和④探究金属规格(铝片,铝粉)对该反应速率的影响; 4.①和⑤实验探究铝与稀盐酸和稀硫酸反应的差异 | ① | 铝片 | ||
② | 25?C | 铝片 | 2.0mol/L盐酸 | |
③ | 35?C | 铝片 | 2.0mol/L盐酸 | |
④ | 铝粉 | |||
⑤ | 25?C | 铝片 | 2.0mol/L硫酸 |
(2)该小组同学在对比①和⑤实验时发现①的反应速度都明显比⑤快,你能对问题原因作出哪些假设或猜想(列出一种即可)?
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二下期中化学试卷(解析版) 题型:选择题
下列有关对定量实验的误差分析正确的是( )
A.中和热测定实验中,缓慢地将NaOH溶液倒入测定装置中——测定结果无影响
B.酸碱中和滴定实验中,盛装标准溶液的滴定管滴定前无气泡而滴定后有气泡——测定结果偏高
C.用排水法收集气体并测定气体体积时,量筒中液面高于集气瓶中液面时——测定结果偏低
D.测定溶液pH的实验中,用干燥的pH试纸测定新制氯水的pH——测定结果无影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com