
【题目】(1)配平该反应化学方程式且回答下列问题:__KMnO4+__HCl=__MnCl2+___KCl+__Cl2↑+__H2O
(2)氧化剂是__,氧化产物是____(填化学式)。
(3)若生成71gCl2,被氧化的HCl是__mol。
【答案】2 16 2 2 5 8 KMnO4 Cl2 2
【解析】
(1)反应中高锰酸钾中+7价锰降为氯化锰中+2价,降价数为5,得到5,mol电子,氯化氢中-1价氯化合价升高为氯气中0价,升高为1,生成1mol氯气失去2mol电子,依据氧化还原反应中得失电子守恒、原子个数守恒配平方程式;
(2)反应中所含元素化合价降低的为氧化剂,生成物中所含元素化合价升高为氧化产物;
(3)依据方程式2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,生成1mol氯气转移2mol电子,被氧化的氯化氢物质的量为2mol,据此解答。
(1)反应中高锰酸钾中+7价锰降为氯化锰中+2价,降价数为5,得到5mol电子,氯化氢中-1价氯化合价升高为氯气中0价,升高为1,生成1mol氯气失去2mol电子,依据氧化还原反应中得失电子守恒,高锰酸钾系数为2,氯气系数为5,依据原子个数守恒,氯化锰系数为2,氯化钾系数为2,依据氯原子个数守恒氯化氢系数为16,水分子系数为8,所以方程式:2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O;
(2)依据(1)分析可知,反应中高锰酸钾中锰元素化合价降低,所以高锰酸钾为氧化剂,化学式KMnO4;生成物中氯气中的氯是由氯化氢中-1价氯化合价升高得到,所以氯气为氧化产物,化学产物Cl2;
(3)71gCl2物质的量为![]() =1mol,依据方程式2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,生成1mol氯气转移2mol电子,被氧化的氯化氢物质的量为2mol。
=1mol,依据方程式2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,生成1mol氯气转移2mol电子,被氧化的氯化氢物质的量为2mol。


科目:高中化学 来源: 题型:
【题目】25 ℃时,用Na2S沉淀Cu2+、Zn2+两种金属阳离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。下列说法不正确的是( )
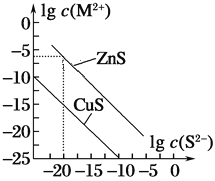
A.向Cu2+浓度为1×10-5 mol·L-1的工业废水中加入ZnS粉末,会有CuS沉淀析出
B.25 ℃时,Ksp(CuS)约为1×10-35
C.向100 mL Zn2+、Cu2+浓度均为1×10-5 mol·L-1的混合溶液中逐滴加入1×10-4 mol·L-1的Na2S溶液,Cu2+先沉淀
D.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种气态烷烃X和一种气态烯烃Y组成的混合物10g,其密度为相同条件下氢气密度的12.5倍,该混合气体通过溴水,使溴水增重8.4g,则X,Y可能是( )
A. 甲烷和丙烯B. 甲烷和乙烯C. 乙烷和乙烯D. 乙烯和丙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯装置,请根据装置回答问题:
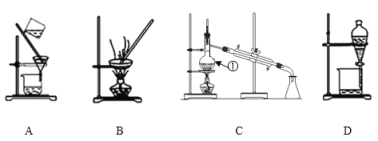
(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是___。
(2)装置C中①的名称是___,此装置中冷凝水进出方向是___(填“上进下出”还是“下进上出”)。装置D中的分液漏斗在使用之前应该___,在分液时为使液体顺利滴下,应进行的具体操作是___。
(3)某硝酸钠固体中混有少量硫酸钠杂质,现设计一实验方案,既除去杂质,又配成硝酸钠溶液。实验方案:先将固体溶于蒸馏水配成溶液,选择合适的试剂和操作完成表格中各步实验。
选择适当试剂按顺序添加 | ① | Na2CO3溶液 | ④ |
实验操作 | ② | ③ | 加热 |
所加入的试剂①可以是___(填化学式),证明溶液中SO42-已经除尽的方法是___。加入Na2CO3溶液的目的是___,所加入的试剂④可以是___(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁粉和氧化亚铁粉末的混合物共9.2克,加入到150毫升的稀硫酸中,恰好完全反应,得到氢气2.24升(标准状况)。求:
(1)混合物中铁的质量?___
(2)原稀硫酸的物质的量浓度?___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A. 1mol甲基含10NA个电子
B. 15 g C2H6中含有共价键数目为3NA
C. 标准状况下,11.2 L三氯甲烷所含的分子数目为0.5NA
D. 一定条件下,2.6 g苯和苯乙烯的混合物完全燃烧消耗O2的分子数为0.25NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把VL含有MgSO4、K2SO4的混合溶液分为两等份,一份加入amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含有bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡,则原混合溶液中钾离子的浓度为( )
A.![]() mol/LB.
mol/LB.![]() mol/LC.
mol/LC.![]() mol/LD.
mol/LD.![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)___gH2O2中所含原子数与0.2molH3PO4所含原子数相等。
(2)同温同压下某容器中分别充满了O2、CO2及某气体X时的质量分别是116g、122g、114g,则气体X的相对分子质量是___。
(3)14.2g无水硫酸钠配制成500毫升溶液,其物质的量浓度为___;若从中取出50毫升溶液,其物质的量浓度为___,若将这50毫升溶液用水稀释到100毫升所得溶液中Na+的物质的量浓度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | W | Y | |
X | 硫 | Z |
回答下列问题:
(1)表中元素原子半径最大的是___(写元素符号),Z原子核外电子能量最高的电子亚层是____。
(2)下列事实能说明Y元素的非金属性比S元素的非金属性强的是_____。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)W的氢化物与F2反应,生成一种铵盐与化合物WF3,WF3的分子构型为三角锥形。
①WF3分子为___〔填“极性”或“非极性”)分子。
②写出该反应的化学方程式,配平并标出电子转移的方向和数目:_____。
(4)硫酸工业生产中接触室内发生的反应方程式为_______;在实际生产中,操作温度选定400~500℃、压强通常采用常压的原因分别是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com