
| A. | 52 | B. | 90 | C. | 142 | D. | 232 |
科目:高中化学 来源: 题型:选择题
| A. | CS2为V形的极性分子 | B. | ClO3-的空间构型为平面三角形 | ||
| C. | SF6中有6对完全相同的成键电子对 | D. | SiF4和SO3的中心原子均为sp2杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
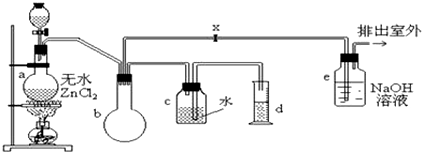
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a-n-3 | B. | a+n+3 | C. | a+n-3 | D. | a-n+3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于分子间作用力的存在,因而CO2在加热条件下不易发生分解 | |
| B. | 非金属原子间不可能形成离子化合物 | |
| C. | 在PCl3分子中各原子都达到8电子稳定结构 | |
| D. | 离子化合物中可能存在共价键,共价化合物中也可能存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Cu3N的晶胞结构如图,N3-的配位数为6,Cu+半径为acm,N3-半径为bcm,Cu3N的密度为$\frac{103}{4{N}_{A}(a+b)^{3}}$g•cm-3.(阿伏加德罗常数用NA表示,Cu、N相对分子质量为64、14)
Cu3N的晶胞结构如图,N3-的配位数为6,Cu+半径为acm,N3-半径为bcm,Cu3N的密度为$\frac{103}{4{N}_{A}(a+b)^{3}}$g•cm-3.(阿伏加德罗常数用NA表示,Cu、N相对分子质量为64、14)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;A、B、D的熔点依次增大的顺序为SiO2>NaF>P4.
;A、B、D的熔点依次增大的顺序为SiO2>NaF>P4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com