
| A.0.1 mo/L | B.1 mo/L | C.0.08 mo/L | D.0.8 mo/L |
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源:不详 题型:填空题
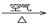 CuO
CuO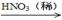 Cu(NO3)2
Cu(NO3)2 | A.40.32L | B.30.24L | C.20.16L | D.13.44L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
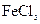 可用作印刷电路铜板腐蚀剂。
可用作印刷电路铜板腐蚀剂。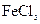 溶液腐蚀印刷电路铜板的离子方程式 。
溶液腐蚀印刷电路铜板的离子方程式 。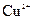 、
、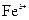 的浓度均为
的浓度均为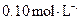 ,不考虑溶液体积的变化,则原
,不考虑溶液体积的变化,则原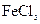 溶液的浓度为 。
溶液的浓度为 。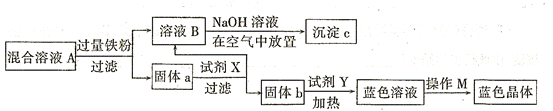
 的操作是
的操作是 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
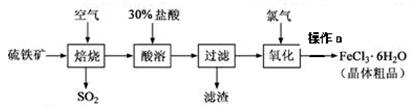
 2SO3,该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为 。
2SO3,该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为 。| A.玻璃棒 | B.烧杯 | C.托盘天平 | D.500mL量筒 |
 溶液吸收,尾气中污染空气的气体为 (写化学式)。
溶液吸收,尾气中污染空气的气体为 (写化学式)。查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 加硫酸的序号 | 每次加入硫酸的体积/mL | 剩余固体的质量/g |
| 1 | 20.0 | 16.0 |
| 2 | 20.0 | 12.0 |
| 3 | 20.0 | 8.0 |
| 4 | 20.0 | 8.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.56(3x+y)g | B.56(3x-y) g | C.28(3x+y)g | D.28(3x-y)g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 a2Fe2O4+ NH3+ NaOH
a2Fe2O4+ NH3+ NaOH Fe3O4+4NaOH
Fe3O4+4NaOH 。若有1mol Na2Fe2O4生成,则反应中有____________mol电子转移。
。若有1mol Na2Fe2O4生成,则反应中有____________mol电子转移。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.称取15.2g硫酸铜固体,加入1000 mL水 |
B.称取2 4g胆矾溶于水配成1000 mL溶液 4g胆矾溶于水配成1000 mL溶液 |
| C.称取16 g硫酸铜固体,加入1000 mL水 |
| D.称取25 g胆矾溶于水配成1000 mL溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com