
| A. | 共价化合物中一定不含离子键 | |
| B. | 离子化合物中一定不含共价键 | |
| C. | 金属越活泼金属键越强 | |
| D. | 双原子分子中共价键越强,沸点越高 |
分析 A.只含共价键的化合物是共价化合物;
B.含有离子键的化合物是离子化合物,离子化合物可能含有共价键;
C.金属性越强,金属键越弱;
D.双原子分子中共价键强弱是决定化学性质,而分子间作用力的强弱是决定物理性质.
解答 解:A.只含共价键的化合物是共价化合物,所以共价化合物中一定不含离子键,故A正确;
B.含有离子键的化合物是离子化合物,离子化合物可能含有共价键,如过氧化钠中既含离子键又含共价,故B错误;
C.金属性强的元素原子核对外层电子吸引力弱,外层电子更活跃,容易脱离原子,从而发生化学反应;金属键就是金属离子和自由电子的相互作用,故C错误;
D.双原子分子中共价键强弱是决定化学性质,而分子间作用力的强弱是决定物理性质,所以沸点高低是分子间作用力的大小决定的,故D错误;
故选A.
点评 本题考查了化合物类型和化学键类型的关系,难度不大,注意相关基础知识的积累.


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后得到NH3分子数为NA | |
| B. | 一定条件下,2.3g的Na完全与O2反应生成3.5g产物时失去的电子数为0.1NA | |
| C. | 1.0L的0.1 mol•L-1Na2CO3溶液中含有的CO32-离子数为0.1NA | |
| D. | 标准状况下,11.2L的CCl4中含有的CCl4分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O含有的分子数为 NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA | |
| C. | 物质的量浓度为1mol/L的MgCl2溶液中,含有Cl-个数为2NA | |
| D. | 通常状况下,NA 个CO2分子占有的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率:4v正(O2)=5v逆(NO) | |
| B. | NH3、O2、NO、H2O的分子个数比是4:5:4:6 | |
| C. | 单位时间内生成4 mol NO的同时消耗6 mol H2O | |
| D. | 反应混合物中NH3的体积分数不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ①②③ | D. | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
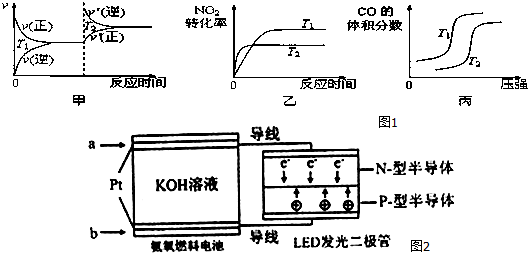
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
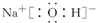 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 碳 | 氮 | Y | |
| X | 硫 | Z |
 ,其中氮的化合价为②-2,实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为③NaClO+2NH3=N2H4+NaCl+H2O .
,其中氮的化合价为②-2,实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为③NaClO+2NH3=N2H4+NaCl+H2O .查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com