
| A. | 石墨转化为金刚石需吸热 | B. | 石墨和金刚石的转化是物理变化 | ||
| C. | 金刚石的稳定性强于石墨 | D. | 石墨和金刚石是同分异构体 |
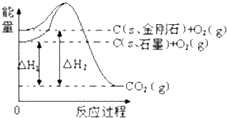
分析 先根据由图得:①C(S,石墨)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
②C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJ•mol-1,然后根据盖斯定律写出石墨转变成金刚石的热化学方程式,根据物质的能量越低越稳定,拆化学键吸收能量,形成化学键放出热量来解答.
解答 解:由图得:①C(S,石墨)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
②C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJ•mol-1,
利用盖斯定律将①-②可得:C(S,石墨)=C(S,金刚石)△H=+1.9kJ•mol-1,则
A、依据热化学方程式 C(S,石墨)=C(S,金刚石)△H=+1.9kJ•mol-1,12g石墨的总键能比1 mol金刚石的总键能大于1.9 kJ,石墨转化为金刚石需吸热,故A正确;
B、石墨转化为金刚石是发生的化学反应,属于化学变化,故B错误;
C、由图象可知,金刚石能量大于石墨的总能量,物质的量能量越大越不稳定,则石墨比金刚石稳定,故C错误;
D、石墨和金刚石是碳元素的不同单质,不是同分异构体,故D错误;
故选A.
点评 本题考查热化学方程式的书写及应用,题目难度不大,注意图象分析和物质的稳定性与能量的关系.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | CCl4、SiCl4、SiH4 | B. | H2S、NCl3、CH4 | ||
| C. | BCl3、CH2═CH2、环己烷 | D. | SO3、C6H6(苯)、CH3C≡CH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 结构决定性质,性质体现结构.对结构和性质的研究是学好化学的基础.
结构决定性质,性质体现结构.对结构和性质的研究是学好化学的基础.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuSO4溶液中:Na+、NH4+、K+、NO3-、Mg2+ | |
| B. | 使酚酞变红色的溶液中:NH4+、Zn2+、Cl-、NO3- | |
| C. | 水电离的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、AlO2-、SO32- | |
| D. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaAt易溶于苯和四氯化碳等有机溶剂 | |
| B. | At的最高化合价为+7价 | |
| C. | At2是一种有色固体,与H2反应十分缓慢 | |
| D. | AgAt是有色固体,见光易分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醇,乙醇 | B. | 乙醇,1-丙醇 | C. | 2-丙醇和1-丁醇 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
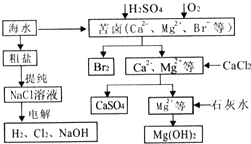 工业上对海水资源综合开发利用的部分工艺流程如图所示.
工业上对海水资源综合开发利用的部分工艺流程如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com