
【题目】锌与100mL 18.5molL-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲35.84L(标准状况)。将反应后的溶液稀释至1L,测得溶液中c(H+)=0.1 mol/L,下列叙述不正确的是( )
A. 反应中共消耗1.8molH2SO4
B. 气体甲中SO2与H2的体积比为7:1
C. 反应中共消耗1.6molZn
D. 反应中共转移3.2mol电子
【答案】B
【解析】生成气体的物质的量为![]() =1.6mol,溶液剩余硫酸的物质的量为
=1.6mol,溶液剩余硫酸的物质的量为![]() ×1L×0.1mol/L=0.05mol,参加反应的n(H2SO4)=0.1L×18.5mol/L-0.05mol=1.8mol,随着反应的进行,硫酸的浓度逐渐减小,设反应生成xmolSO2,ymolH2,根据Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O、Zn+H2SO4(稀)=ZnSO4+H2↑有:x+y=1.6,2x+y=1.8,解之得 x=0.2,y=1.4,所以反应会生成0.2mol的二氧化硫和1.4mol的氢气。A.由以上计算可知,反应中共消耗1.8molH2SO4,故A正确;B.气体甲为SO2和H2的混合物,且V(SO2):V(H2)= n(SO2):n(H2)=1:7,故B错误;C.反应中共消耗金属Zn的质量n(Zn)=0.2mol+1.4mol =1.6mol,故C正确;D.在反应Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O中,生成0.2mol的二氧化硫转移电子为0.4mol,反应Zn+H2SO4(稀)=ZnSO4+H2↑中,生成1.4mol氢气转移电子2.8mol,所以反应中共转移3.2mol电子,故D正确;故选B。
×1L×0.1mol/L=0.05mol,参加反应的n(H2SO4)=0.1L×18.5mol/L-0.05mol=1.8mol,随着反应的进行,硫酸的浓度逐渐减小,设反应生成xmolSO2,ymolH2,根据Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O、Zn+H2SO4(稀)=ZnSO4+H2↑有:x+y=1.6,2x+y=1.8,解之得 x=0.2,y=1.4,所以反应会生成0.2mol的二氧化硫和1.4mol的氢气。A.由以上计算可知,反应中共消耗1.8molH2SO4,故A正确;B.气体甲为SO2和H2的混合物,且V(SO2):V(H2)= n(SO2):n(H2)=1:7,故B错误;C.反应中共消耗金属Zn的质量n(Zn)=0.2mol+1.4mol =1.6mol,故C正确;D.在反应Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O中,生成0.2mol的二氧化硫转移电子为0.4mol,反应Zn+H2SO4(稀)=ZnSO4+H2↑中,生成1.4mol氢气转移电子2.8mol,所以反应中共转移3.2mol电子,故D正确;故选B。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】室温下,将1.000molL﹣1盐酸滴入20.00mL 1.000molL﹣1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( ) 
A.a点由水电离出的c(H+)=1.0×10﹣14molL﹣1
B.b点:c(NH4+)+c(NH3H2O)=c(Cl﹣)
C.c点:c(Cl﹣)=c(NH4+)
D.d点后,溶液温度略下降的主要原因是NH3H2O电离吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有Al、C12、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )
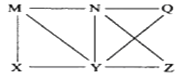
A. N一定是HCl(aq) B. X可能为Al或C12
C. Y一定为NaOH(aq) D. Q、Z中的一种必定为Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种黄酮类化合物的中间体,其结构简式如图所示。下列有关化合物X的说法正确的是

A. 该有机物分子式为C24H22O5
B. 能发生取代反应、加成反应和氧化反应
C. 1mol化合物X最多能与2mol NaOH反应
D. 1mol化合物X最多可与11mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验某卤代烃(R﹣X)中的X元素,有下列实验操作:①加热煮沸;②加入AgNO3溶液;③取少量卤代烃;④加入稀硝酸酸化;⑤加入NaOH溶液;⑥冷却.正确操作的先后顺序是( )
A.③①⑤⑥②④
B.③①②⑥④⑤
C.③⑤①⑥④②
D.③⑤①⑥②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年3月21日是第二十五届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品1L,进行了三组实验,其操作和有关图像如下所示:

请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的阴离子是__________,一定存在的阳离子是______________________。
(2)写出实验③图像中沉淀达到最大量且质量不再发生变化阶段发生反应的离子反应方程式:_____________________________________________。
(3)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为___________,所得沉淀的最大质量是_________g。
(4)若通过实验确定原废水中c(Na+)=0.18 mol·L-1,试判断原废水中NO3-是否存在?__________(填“存在”“不存在”或“不确定”)。若存在,c(NO3-)=____________ mol·L-1。(若不存在或不确定则此空不填)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲、乙两烧杯中的溶液,分别含有大量的Fe3+、K+、H+、Cl-、CO32-、OH-离子中的3种(每种离子不重复使用),已知甲烧杯中的溶液呈黄色,则乙烧杯的溶液中大量存在的离子可能是
A.K+、OH-、CO32-B.CO32-、OH-、Cl-
C.K+、H+、Cl-D.Fe3+、H+、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com