
| A. | 道尔顿发现原子--“空心球”模型 | |
| B. | 汤姆逊发现电子--“葡萄干布丁”模型 | |
| C. | 卢瑟福进行α粒子散射实验--“核式”模型 | |
| D. | 玻尔解释氢原子光谱--“电子分层排布”模型 |
分析 A.英国科学家道尔顿建立近代原子模型-“实心球”模型;
B.汤姆孙提出原子的葡萄干面包模型;
C.卢瑟福提出原子的核式结构模型;
D.玻尔的原子模型中电子轨道和原子的能量都是量子化的,是建立在三个基本假设的基础上的理论.
解答 解:A.道尔顿发现原子--“实心球”模型,故A错误;
B.汤姆孙根据实验发现了电子,而且原子呈电中性,据此提出原子的葡萄干面包模型,故B正确;
C.卢瑟福提出原子的核式结构模型,这一模型建立的基础是α粒子散射实验,故C正确;
D.1913年丹麦物理学家波尔(卢瑟福的学生)引入量子论观点,提出电子在一定轨道上运动的原子结构模型,原子系统只能具有一系列的不连续的能量状态,当原子从一个具有较大能量的定态跃迁到另一个能量较低的定态时,它辐射出具有一定频率的光子,原子的不同能量状态和电子沿不同的圆形轨道绕核运动相对应,氢原子光谱指的是氢原子内的电子在不同能阶跃迁时所发射或吸收不同波长,该光谱的发现在玻尔核外电子分层排布模型原子结构的认识过程中,有极为重要的意义,故D正确.
故选A.
点评 本题考查了原子的结构和化学史,题目难度不大,注意基础知识的积累,注意玻尔原子模型:电子的轨道量子化,原子的能量量子化.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu和AgNO3溶液反应:Cu+Ag+═Cu2++Ag | |
| B. | 往AlCl3溶液中滴入氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 铁与稀盐酸反应:Fe+2H+═Fe2++H2↑ | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol/L的CH3COOH溶液中加入少量CH3COONa固体,溶液pH增大 | |
| B. | 在密闭容器中充入一定量NO2建立2NO2(g)?N2O4(g)平衡后,增大压强,体系颜色加深 | |
| C. | 向水中投入金属Na,最终溶液呈碱性 | |
| D. | 在滴有酚酞的Na2CO3溶液中,慢慢滴入BaCl2溶液,溶液的红色逐渐褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
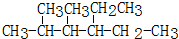
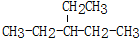 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 待测气体 | 敏感电极部分产物 |
| NO2 | NO |
| Cl2 | HCl |
| CO | CO2 |
| H2S | H2SO4 |
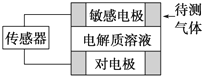
| A. | 上述气体检测时,敏感电极均作原电池正极 | |
| B. | 检测Cl2气体时,敏感电极的电极反应为2Cl--2e-═Cl2 | |
| C. | 检测H2S气体时,对电极充入空气,对电极上电极反应式为O2+2H2O+4e-═4OH- | |
| D. | 检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小不相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com