
科目:高中化学 来源:2016届甘肃省高三上学期第二次月考理综化学试卷(解析版) 题型:填空题
(14分)铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石的混合物。某化学兴趣小组从铁砂中分离出磁性氧化物,并进行铝热反应实验。
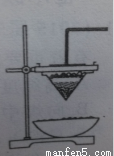 (1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是_________________现象很壮观,取少许生成的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现结果的原因,除了可能混有没有反应的磁性氧化铁外,还有一个原因是____________设计一个简单的实验方案,证明上述所得“铁块”中含有金属铝。该实验所用的试剂 是____________,反应的离子方程式_____________________
(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是_________________现象很壮观,取少许生成的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现结果的原因,除了可能混有没有反应的磁性氧化铁外,还有一个原因是____________设计一个简单的实验方案,证明上述所得“铁块”中含有金属铝。该实验所用的试剂 是____________,反应的离子方程式_____________________
(2)写出此铝热反应的化学方程式:___________________________每摩尔单质铝参与反应,转移的电子数为___________________
(3)除磁性氧化铁可做铝热反应实验外,下列哪些试剂也可以( )
A.CuO B.Na2O2 C .MnO2 D.MgO
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实验图示转化关系的是
选项 | W | X | Y | Z |
|
A | S | SO2 | SO3 | H2SO4 | |
B | Na | Na2O2 | NaOH | NaCl | |
C | Al | AlCl3 | NaAlO2 | Al2(SO4)3 | |
D | Fe | FeCl3 | Fe(OH)2 | FeCl2 |
查看答案和解析>>
科目:高中化学 来源:2016届安徽省安庆市高三上学期第一次质检化学试卷(解析版) 题型:填空题
(10分)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
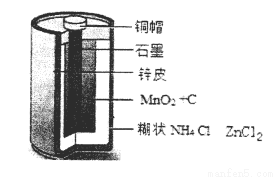
(1)该电池的负极材料是 电池工作时,电子从Zn极流向 填(“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是 。
欲除去Cu2+,最好选用下列试剂中的 (填代号)。
A.NaOH B.Zn C.Fe D.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液制取,则MnO2在 极产生。阴极的电极反应式是 。若电解电路中通过2mol电子,MnO2的理论产量为 g。(MnO2的摩尔质量为:87g/mol)
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期第二次月考化学试卷(解析版) 题型:选择题
25 ℃时,下列各组离子在指定溶液中一定能大量共存的是
A.pH=1的溶液中:Na+、K+、MnO4-、CO32-
B.c(H+)=1×10-13 mol·L-1的溶液中:Mg2+、Cu2+、SO42-、NO3-
C.0.1 mol·L-1 NH4HCO3溶液中:K+、Na+、NO3-、Cl-
D.0.1 mol·L-1 FeCl3溶液中:Fe2+、NH4+、SCN-、SO42-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上学期第一次月考化学试卷(解析版) 题型:填空题
完成以下四个小题:
(1)请完成下列各空:
①pH= a的CH3COOH溶液稀释100倍后所得溶液pH a +2(填“>”或“<”)
②0.01mol/LCH3COOH溶液的pH 2(填“>”或“<”);
③0.1mol/LCH3COONa溶液的pH 7(填“>”或“<”);
(2)观察比较以上三个小题,试猜想证明某酸(HA)是弱电解质的原理有两个:
一是: ;
二是: 。
(3)请你根据以上原理提出一些方案,证明HA酸是弱电解质:(只需简明写出方案,不需写出具体步骤,以下项目可不填满也可增加项目)
①
②
查看答案和解析>>
科目:高中化学 来源:2016届河北省邯郸市高三上学期10月月考化学试卷(解析版) 题型:选择题
250 mL K2SO4和CuSO4的混合溶液中c(SO42-)=0.5 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到1.12 L气体(标准状况下)。假定电解后溶液体积仍为250 mL,下列说法不正确的是
A.电解得到Cu的质量为3.2 g
B.上述电解过程中共转移电子0.2 mol
C.电解后的溶液中c(H+)=0.2 mol·L-1
D.原混合溶液中c(K+)=0.6 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上学期10月月考化学试卷(解析版) 题型:填空题
(12分) 某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。用pH计测定25 ℃时不同浓度的醋酸的pH,其结果如下:
醋酸浓度/mol·L-1 | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列问题:
(1)写出醋酸的电离方程式:__________________________。
(2)醋酸溶液中存在的微粒有__________________________。
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是__________________。
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度(选填“增大”“减小”或“不变”)__________。
(5)常温常压下,在 pH =5的稀醋酸溶液中,c(CH3COO-)= (精确值,用表达式表示)。
(6)下列方法中,可以使0.10 mol·L-1 CH3COOH溶液中CH3COOH电离程度增大的是 。
a.加入少量0.10 mol·L-1的稀盐酸
b.加入少量冰醋酸
c.加入少量氯化钠固体
d.加热CH3COOH溶液
e.加入Zn粒
f.加入少量0.10 mol·L-1的CH3COONa溶液
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期第一次检测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.摩尔是用来衡量微观粒子多少的一种物理量
B.在一定的温度和压强下,各种气体的摩尔体积相等
C.阿伏加德罗常数的数值是0.012 kg 14C所含的原子个数
D.若气体摩尔体积为22.4 L•mol﹣1,则所处条件为标准状况
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com