
【题目】某同学用下列装置制备并检验Cl2的性质。

下列说法正确的是
A. Ⅰ图中:如果MnO2过量,浓盐酸就可全部被消耗
B. Ⅱ图中:量筒中发生了加成反应
C. Ⅲ图中:生成蓝色的烟
D. Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】1869年,门捷列夫所制出的第一张元素周期表,是将元素按照下列的哪个量从小到大排列的
A. 核电荷数 B. 质子数 C. 质量数 D. 相对原子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。回答下列问题:
(1)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol -1
2SO3(g) ΔH=-196.6 kJ·mol -1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g) 的ΔH= kJ·mol-1。
SO3(g)+NO(g) 的ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中发生上述反应,下列能说反应达到平衡状态的有 。(填字母)
a.体系密度保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1:5,则平衡常数K= 。
(2)CO可用于合成甲醇,反应的化学方程式为 CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。

(3)一种用NH3脱除烟气中NO的原理如下图:

①该脱硝原理中,NO最终转化为H2O和 (填化学式)。
②当消耗1 mol NH3和0.5 molO2时,除去的NO在标准状况下的体积为 。
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,反应物与生成物三者的物质的量之比比3:1:1,则该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另—份中逐渐加入铁粉,产生气体的量随铁粉质量的增加的变化关系如图所示(已知硝酸只被还原为 NO气体)。下列分析或结果错误的是

A. 原混合酸中NO3-的物质的量为0.1mol
B. 第二份溶液中最终溶质为FeSO4
C. OA段产生的是NO,AB段的反应为Fe+2Fe3+==3Fe2+,BC段产生氢气
D. H2SO4浓度为2.5 molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活和环境密切相关。下列有关说法正确的是
A. 编织渔网的尼龙绳的主要成分是纤维素
B. 文房四宝中的砚台,用石材磨制的过程是化学变化
C. 丝绸的主要成分是蛋白质,它属于天然高分子化合物
D. 月饼中的油脂易被氧化,保存时常放入装有硅胶的透气袋
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】沼气是一种能源,它的主要成分是CH4。0.5 mol CH4完全燃烧生成CO2和液态水时放出445 kJ的热量,则下列热化学方程式中正确的是
A. 2CH4(g)+4O2(g)===2CO2(g)+4H2O(l) ΔH=+890 kJ·mol-1
B. CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=+890 kJ·mol-1
C. CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
D. ![]() CH4(g)+O2(g)===
CH4(g)+O2(g)===![]() CO2(g)+H2O(l) ΔH=-890 kJ·mol-1
CO2(g)+H2O(l) ΔH=-890 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是
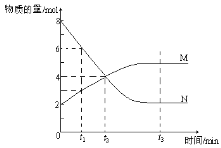
A.反应的化学方程式为:2 M![]() N
N
B.t1时,N的浓度是M浓度的2倍
C.t2时,正逆反应速率相等,达到平衡
D.t3时,正反应速率大于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
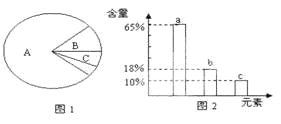
A. 若图1表示正常细胞,则A、B化合物共有的元素中含量最多的是a
B. 若图1表示细胞完全脱水后化合物含量扇形图,则A中含量最多的元素为图2的b
C. 上图2中数量最多的元素是碳元素,这与细胞中含量最多的化合物有关
D. 若图1表示正常细胞,则B化合物具有多样性,其必含的元素为C、H、0、N
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com