
(10分)有一混合物的水溶液,只可能含以下离子中的若干种:K+ 、Al3+ 、Fe3+ 、Mg2+ 、Ba2+ 、 NH4+、Cl- 、CO32-、SO42 -,现取三份100 mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生。
②第二份加过量NaOH溶液加热后收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。
③在甲溶液中通过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。
④第三份加足量BaCl2溶液后得白色沉淀,沉淀经足量盐酸洗涤干燥后质量为11.65 g。
根据上述实验回答:
(1)一定不存在的离子是___________,不能确定是否存在的离子是_____________。
(2)试确定溶液中肯定存在的阴离子及其浓度(可不填满):
离子符号______,浓度__________________;
离子符号______,浓度__________________;
离子符号______,浓度__________________;
(3)试确定K+ 是否存在________(填“是”或“否”),判断的理由是__________。
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源:2016届辽宁省大连市高三期初考试化学试卷(解析版) 题型:选择题
碳与浓硫酸共热产生的气体X和铜与浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法不正确的是
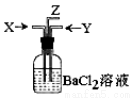
A.洗气瓶中产生的沉淀是碳酸钡
B.在Z导管出来的气体中有二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡
D.在Z导管口有红棕色气体出现
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
在下列实验操作中均用到的仪器是
①配制一定物质的量浓度的溶液;②用pH试纸检验溶液酸碱度;③过滤;④蒸发
A.试管 B.漏斗
C.胶头滴管 D.玻璃棒
查看答案和解析>>
科目:高中化学 来源:2016届山东省枣庄市高三9月阶段性学情检测化学试卷(解析版) 题型:填空题
向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式:__________________。
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液中显中性
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的_______曲线表示(填序号)。

(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将___ 。

查看答案和解析>>
科目:高中化学 来源:2016届山东省枣庄市高三9月阶段性学情检测化学试卷(解析版) 题型:选择题
对下列物质用途的解释不正确的是
A | B | C | D | |
用途 | 抗坏血酸(Vc)可作抗氧化剂 | 明矾可用于净水 | 纯碱可去油污 | “84”消毒液可用于漂白 |
解释 | Vc具有酸性 | 明矾在水中生成的氢氧化铝胶体具有吸附性 | 纯碱水解呈碱性 | 置于空气中生成的次氯酸有强氧化性 |
查看答案和解析>>
科目:高中化学 来源:2016届山东省新高三开学初模拟检测化学试卷(解析版) 题型:选择题
用丙醛(CH3-CH2-CHO)制聚丙烯  CH2-CH(CH3)
CH2-CH(CH3) 过程中发生的反应类型为
过程中发生的反应类型为
①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原
A.①④⑥ B.⑤②③ C.⑥②③ D.②④⑤
查看答案和解析>>
科目:高中化学 来源:2016届山东省新高三开学初模拟检测化学试卷(解析版) 题型:选择题
下列热化学方程式或离子方程式正确的是
A.已知H2的标准燃烧热ΔH=-285.8 kJ·mol-1,则用热化学方程式可表示为:
H2(g)+1/2O2(g)===H2O(g)ΔH=-285.8 kJ·mol-1
B.NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O===Fe(OH)2↓+2HClO
C.NH4HSO3溶液与足量NaOH溶液共热:NH4++H++2OH- NH3↑+2H2O
NH3↑+2H2O
D.用足量KMnO4溶液吸收SO2气体:2MnO4-+5SO2+2H2O===2Mn2++5SO42-+4H+
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:填空题
化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。请推测并回答:
(1)甲的化学式__________。
(2)甲与AlCl3反应得到NaAlH4的化学方程式__________。
(3)NaAlH4与水发生氧化还原反应的化学方程式__________。
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高一下学期期末考试化学试卷(解析版) 题型:选择题
如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是
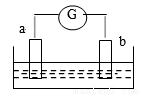
A、a为负极,是铁片,烧杯中的溶液为硫酸
B、b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C、a为正极,是碳棒,烧杯中的溶液为硫酸
D、b为正极,是碳棒,烧杯中的溶液 为硫酸铜溶液
为硫酸铜溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com