
在体积不变的密闭容器中,2A(g)+2B(g) 3C(g)+D(g)达到平衡状态的标志是.
3C(g)+D(g)达到平衡状态的标志是.
A.单位时间内生成2n mol A,同时生成n mol D
B.容器内压强不随时间而变化
C.单位时间内生成n mol B,同时消耗1.5n mol C
D.容器内混合气体密度不随时间而变化
科目:高中化学 来源: 题型:
某有机物M是合成药物的中间体,其结构如右图所示,下列说法不正确的是( )
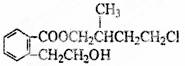 A.M属于芳香族化合物
A.M属于芳香族化合物
B.M的分子式为C14H19O3Cl
C.1 mol M最多能消耗3 mol NaOH
D.M能发生取代、加成、消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
(2013·北京理综,27)用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解Al2O3的离子方程式是_________________________________________
________________________________________________________________________。
(2)将MnO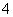 氧化Fe2+的离子方程式补充完整:
氧化Fe2+的离子方程式补充完整:
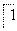 MnO
MnO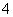 +
+ Fe2++
Fe2++ ________===
________===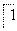 Mn2++
Mn2++ Fe3++
Fe3++ ________。
________。
(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释步骤Ⅱ的目的___________________________________________。
(4)已知:一定条件下,MnO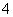 可与Mn2+反应生成MnO2。
可与Mn2+反应生成MnO2。
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是 ________________________________________________________________________。
②Ⅳ中加入MnSO4的目的是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
沼气是一种能源,它的主要成分是CH4,0.5 mol CH4完全燃烧生成CO2和H2O(l)时,放出445 kJ热量,则下列热化学方程式中正确的是
A.2CH4(g)+4O2(g)===2CO2(g)+4H2O(l) ΔH=+890 kJ/mol
B.CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=+890 kJ/mol
C.CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ/mol
D.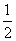 CH4(g)+O2(g)===
CH4(g)+O2(g)===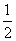 CO2(g)+H2O(l) ΔH=-890 kJ/mol
CO2(g)+H2O(l) ΔH=-890 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
上海人张霞昌在芬兰发明了“纸电池”,这种一面镀锌、一面镀二氧化锰的超薄电池在使用印刷与压层技术后,变成一张可任意裁剪大小的“电纸”,纸内的离子“流过”水和氧化锌组成的电解质溶液,电池总反应式为:
Zn+2MnO2+H2O===ZnO+2MnOOH。下列说法正确的是
A.该电池的正极材料为锌
B.该电池反应中二氧化锰发生了氧化反应
C.电池的正极反应式为MnO2+H2O+e-===MnOOH+OH-
D.当有0.1 mol锌溶解时,流经电解质溶液的电子数为1.204×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中存在下列平衡:
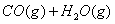
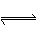
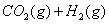 。
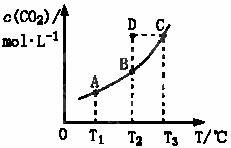
。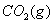 的平衡物质的量浓度
的平衡物质的量浓度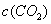 与温度T的关系如右图所示。下列说法错误的是
与温度T的关系如右图所示。下列说法错误的是
A.反应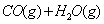
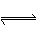
 的
的
B.在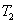 时,若反应处于状态
时,若反应处于状态 ,则一定有v(逆)>v(正)
,则一定有v(逆)>v(正)
C.平衡状态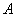 与
与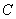 相比,平衡状态
相比,平衡状态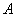 的
的 小
小
D.若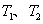 时的平衡常数分别为
时的平衡常数分别为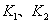 ,则
,则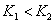
查看答案和解析>>
科目:高中化学 来源: 题型:
还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下:
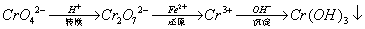
己知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)  Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
A.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g
B.溶液颜色保持不变,说明上述可逆反应达到达平衡状态
C.常温下转换反应的平衡常数K=1×1014,则转化后所得溶液的pH=6
D.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素A、B、C、D的原子序数依次递增.其中A、B、C二种元素基态原子的2p能级上都有未成对电子.且未成对电子个数分别是2、3、2;D与C 可以形成D2C和D2C2两种化合物。回答下列问题:
(1)已知A元素与氢元素形成的某种气态化合物在标准状况下的密度为1.1 6 1 g·L-1,则在该化合物的分子中A原子的杂化方式为 。
(2)A、B、C二种元素的第一电离能由小到大的顺序为 (填元素符号)。
 (3)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子
(3)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子
所需要的能量称为第二电离能I2,依次还有I3、I4、I5……,推测D元素
的电离能第一次突增应出现在第 电离能。
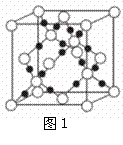
(4)AC2在高温高压下所形成的晶体其晶胞如图1所示。
该晶体的类型属于 晶体.该品体中A原子轨道的
杂化类型为 。
(5)A和C形成原子个数比为1:3的常见离子.推测这种微粒的空间
 构型为 。
构型为 。
(6)C和D形成的一种离子化合物D2C的晶胞结构如图2所示.该晶体
中阳离子的配位数为 。距一个阴离子周围最近的所有阳离子为顶点
构成的几何体为 。已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数为NA.
则晶胞边长a= cm(用含ρ、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)
(1) 的名称是
的名称是
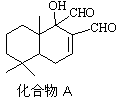
(2)写出右图化合物A中含氧官能团的名称
(3)某物质的实验式是Co(NH3)5BrSO4,向它的溶液中加入BaCl2溶液时,无明显现象;加入强碱处理,也无气体放出。若加入 AgNO3溶液时,产生淡黄色沉淀。写出它的配位化学式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com