
| 推测 | 操作和现象 | 结论 |
| 杂质中的正盐成分可能有: Na2S、Na2CO3 Na2SO4 及Na2SO3 | ①取Wg产品配成稀溶液; ②向溶液中滴加过量BaCl2溶液,有白色沉淀生成,过滤,得沉淀和滤液; ③向沉淀中加入过量盐酸,沉淀完全溶解,并有刺激性气味的气体产生. | 产品杂质中: 一定含有Na2SO3, 可能含有Na2CO3, 一定不含有Na2S、Na2SO4. |
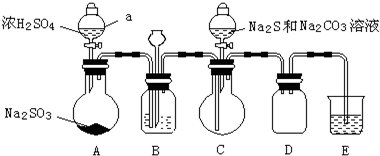
分析 (1)浓硫酸与亚硫酸钠反应生成二氧化硫和硫酸钠;
(2)①装置B中所盛放的液体应不能够与二氧化硫反应;
②如使SO2缓慢进入烧瓶C,应使A中缓慢反应;
(3)①据得失电子守恒和原子守恒配平化学方程式;
②先使C中充满二氧化硫,C中才能反应;
(4)①取Wg产品配成稀溶液;
②向溶液中滴加过量BaCl2溶液,有白色沉淀生成,说明杂志可能有Na2CO3、Na2SO3、Na2SO4,
③向沉淀中加入过量盐酸,沉淀完全溶解,并有刺激性气味的气体产生,说明没有Na2SO4,一定有Na2SO3,可能有Na2CO3.
解答 解:(1)浓硫酸与亚硫酸钠反应生成二氧化硫和硫酸钠,反应方程式为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,故答案为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;
(2)①装置B中所盛放的液体应不能够与二氧化硫反应,二氧化硫能够溶于水,能够与亚硫酸钠和碳酸氢钠溶液反应,故答案为:C;
②如使SO2缓慢进入烧瓶C,应使A中缓慢反应,可观察B的气泡流速,旋转A分液漏斗活塞,通过控制硫酸流量而控制SO2流量,故答案为:观察B的气泡流速,旋转A分液漏斗活塞,通过控制硫酸流量而控制SO2流量;
(3)①S元素在二氧化硫中为+4价,在硫化钠中为-2价,反应后为+2价,所以二氧化硫和硫化钠物质的量之比为2:1,据原子守恒,二氧化硫钱的化学计量数为4,硫化钠的化学计量数为2,据原子守恒,还生成二氧化碳,化学方程式为4SO2+2Na2S+Na2CO3=3Na2S2O3+CO2,故答案为:4;2;1;3;CO2;
②排除装置内空气,先使C中充满二氧化硫,防止发生氧化生成Na2SO4,故答案为:排除装置内空气,防止发生氧化生成Na2SO4;
(4)向溶液中滴加过量BaCl2溶液,有白色沉淀生成,说明杂质可能有Na2CO3、Na2SO3、Na2SO4,向沉淀中加入过量盐酸,沉淀完全溶解,并有刺激性气味的气体产生,说明没有Na2SO4、Na2S,一定有Na2SO3,可能有Na2CO3,排除Na2S的原因是Na2S和Na2SO3在酸性条件下会生成淡黄色的S沉淀,故答案为:
| 推测 | 操作和现象 | 结论 |
Na2SO3 | Na2SO3 Na2CO3 Na2S、Na2SO4 |
点评 本题以制备硫代硫酸钠晶体(Na2S2O3•5H2O)为载体,考查了氧化还原反应方程式书写、配平以及物质的分离提纯、检验、设计优化等,综合性较强,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | CO2、CO、O2、CaO | B. | O2、CO、CO2、CaCO3 | C. | O2、CO2、CO、CaCO3 | D. | CO、CO2、O2、Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
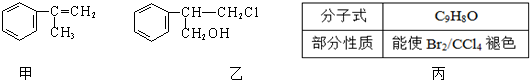
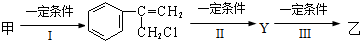
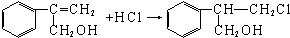 (不需注明反应条件).
(不需注明反应条件).
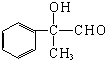 ;丙的结构简式为
;丙的结构简式为 .
. 、
、 、
、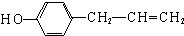 其中一种.
其中一种.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、Ca(ClO)2(aq)$\stackrel{CO_{2}}{→}$HClO(aq)$\stackrel{光照}{→}$HCl(aq) | |
| B. | NH3$→_{催化剂△}^{O_{2}}$NO$\stackrel{O_{2}}{→}$NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| C. | Fe$→_{△}^{少量Cl_{2}}$FeCl2$\stackrel{NaOH溶液}{→}$Fe(OH)2$\stackrel{空气中放置}{→}$Fe(OH)3 | |
| D. | H2SiO3$\stackrel{△}{→}$SiO2$\stackrel{NaOH(aq)}{→}$Na2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验操作 | 目的 |
| A | 取4gNaOH固体溶入100mL水中 | 配制4mol•L-1NaOH溶液 |
| B | 向沸水中逐滴加入1~2mLFeCl3饱和溶液,搅拌并继续煮沸出现浑浊 | 制备Fe(OH)3胶体 |
| C | 测定等物质的量浓度的盐酸、硝酸的pH | 比较Cl、N的非金属性强弱 |
| D | 用熔融氧化铝、CCl4做导电性实验 | 验证两者是离子化合物还是共价化合物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
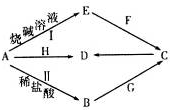
 ,实验室制取G的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
,实验室制取G的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.| O=O(g) | H-H(g) | H-O(g) | |
| 键能/kJ•mol-1 | 496 | x | 463 |
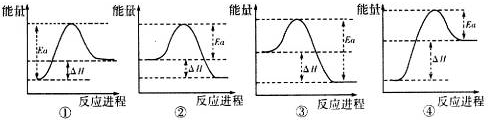
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 反应②的条件是氢氧化钠水溶液、加热
反应②的条件是氢氧化钠水溶液、加热

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 依据氧化还原反应:Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)设计成如图所示的原电池,则关于该电池装置的说法中不正确的是( )
依据氧化还原反应:Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)设计成如图所示的原电池,则关于该电池装置的说法中不正确的是( )| A. | 电极X的材料是Fe | |
| B. | 电解质溶液Y是AgNO3溶液 | |
| C. | 原电池工作时,X电极反应为:Fe-2e-=Fe2+ | |
| D. | 原电池工作时,盐桥中的阴离子不断移向左池的氯化钠溶液中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com