
| ŹµŃéÄŚČŻ | ŹµŃéĻÖĻó | ÓŠ¹Ų·“Ó¦µÄ·½³ĢŹ½»ņ½įĀŪ |
| ¢ŁČ”Ä„¹āŗóĆ¾ĢõÓėĀĮĢõ£¬·Ö±šĶ¶ČėĻ”ŃĪĖįÖŠ | Mg+2HCl=MgCl2+H2”ż 2Al+6HCl=2AlCl3+3H2”ż ĖµĆ÷½šŹōŠŌµÄĒæČõĖ³ŠņĪŖ£ŗMg£¾Al | |
| ¢ŚĻņMgCl2”¢AlCl3ČÜŅŗÖŠ·Ö±šÖšµĪµĪČėNaOHČÜŅŗÖĮ¹żĮæ | ÓėMgCl2ČÜŅŗ·“Ó¦²śÉś°×É«³Įµķ£¬ÓėAlCl3ČÜŅŗ·“Ó¦ĻČ²śÉś°×É«³Įµķ£¬¶ųŗó³ĮµķĶźČ«Čܽā | AlCl3ČÜŅŗÓėNaOHČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗAlCl3+3NaOH=Al£ØOH£©3”ż+3NaCl£¬Al£ØOH£©3+NaOH=NaAlO2+2H2O |
| ¢ŪĻņŠĀÖʵÄNa2SČÜŅŗÖŠµĪČėŠĀÖʵÄĀČĖ® | Éś³Éµ»ĘÉ«µÄ³Įµķ | ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗNa2S+Cl2=S”ż+2NaCl |
| ¢ÜĻņø÷ĪŖ1mol/LµÄH2SO4”¢H3PO4ČÜŅŗÖŠĶ¶ČėĆ¾Ģõ | Ć¾ÓėH2SO4·“Ó¦øü¾ēĮŅ£¬ŃøĖŁ²śÉś“óĮæĪŽÉ«ĘųĢå | ĖµĆ÷·Ē½šŹōŠŌµÄĒæČõĖ³ŠņĪŖ£ŗS£¾P |
·ÖĪö ¢ŁĆ¾ĀĮ±ķĆę¶¼ÓŠĘųÅŻĆ°³ö£¬Ć¾ĀĮČܽā£¬½šŹōŗĶĶ¬ÅØ¶ČµÄĖį·“Ó¦Ō½æģĖµĆ÷½šŹōŠŌŌ½Ē棻
¢ŚĒāŃõ»ÆĀĮŹĒĮ½ŠŌĒāŃõ»ÆĪļ£¬ŗĶĒæĖįĒæ¼ī¶¼ÄÜ·¢Éś·“Ó¦£»
¢ŪĮņ»ÆÄĘŗĶĀČĘų·“Ӧɜ³ÉĮņµ„ÖŹŗĶĀČ»ÆÄĘ£»
¢Ü×īøß¼Ūŗ¬ŃõĖįĖįŠŌŌ½Ēæ¶ŌÓ¦·Ē½šŹōŠŌŌ½Ē森
½ā“š ½ā£ŗ¢ŁČ”Ä„¹āŗóĆ¾ĢõÓėĀĮĢõ£¬·Ö±šĶ¶ČėĻ”ŃĪĖįÖŠ£¬·¢Éś·“Ó¦Mg+2HCl=MgCl2+H2”ż£¬2Al+6HCl=2AlCl3+3H2”ż£¬Ć¾ĀĮ±ķĆę¶¼ÓŠĘųÅŻĆ°³ö£¬Ć¾ĀĮČܽā£¬Ć¾Ģõ·“Ó¦¾ēĮŅĆ°³öĘųÅŻĖŁĀŹæģ£¬ĖµĆ÷Ć¾ŗĶŃĪĖį·“Ó¦æģ£¬½šŹōŠŌµÄĒæČõĖ³ŠņĪŖ£ŗĆ¾µÄ½šŹōŠŌ“óÓŚĀĮµÄ½šŹōŠŌ£¬
¹Ź“š°øĪŖ£ŗMg£¾Al£»
¢ŚĻņMgCl2”¢AlCl3ČÜŅŗÖŠ·Ö±šÖšµĪµĪČėNaOHČÜŅŗÖĮ¹żĮ棬ÓėMgCl2ČÜŅŗ·“Ó¦²śÉś°×É«³Įµķ£¬ÓėAlCl3ČÜŅŗ·“Ó¦ĻČ²śÉś°×É«³Įµķ£¬¶ųŗó³ĮµķĶźČ«Čܽā£¬ĒāŃõ»ÆĀĮŹĒĮ½ŠŌ·ŪĖé·“Ó¦ĒāŃõ»ÆĪļ£¬ŗĶĒæĖįĒæ¼ī¶¼ÄÜ·¢Éś·“Ó¦£¬AlCl3ČÜŅŗÓėNaOHČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗAlCl3+3NaOH=Al£ØOH£©3”ż+3NaCl£¬Al£ØOH£©3+NaOH=NaAlO2+2H2O£¬
¹Ź“š°øĪŖ£ŗAl£ØOH£©3+NaOH=NaAlO2+2H2O£»
¢ŪĻņŠĀÖʵÄNa2SČÜŅŗÖŠµĪČėŠĀÖʵÄĀČĖ®£¬Éś³Éµ»ĘÉ«µÄ³Įµķ£¬Įņ»ÆÄĘŗĶĀČĘų·“Ӧɜ³ÉĮņµ„ÖŹŗĶĀČ»ÆÄĘ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗNa2S+Cl2=S”ż+2NaCl£¬
¹Ź“š°øĪŖ£ŗNa2S+Cl2=S”ż+2NaCl£»
¢ÜĻņø÷ĪŖ1mol/LµÄH2SO4”¢H3PO4ČÜŅŗÖŠĶ¶ČėĆ¾Ģõ£¬Ć¾ÓėH2SO4·“Ó¦øü¾ēĮŅ£¬ŃøĖŁ²śÉś“óĮæĪŽÉ«ĘųĢ壬×īøß¼Ūŗ¬ŃõĖįĖįŠŌŌ½Ēæ¶ŌÓ¦·Ē½šŹōŠŌŌ½Ē棬ĖµĆ÷·Ē½šŹōŠŌµÄĒæČõĖ³ŠņĪŖS£¾P£¬¹Ź“š°øĪŖ£ŗS£¾P£»
µćĘĄ ±¾Ģāæ¼²éĮĖĢ½¾æµŚČżÖÜĘŚŌŖĖŲŠŌÖŹµŻ±ä¹ęĀÉ”¢½šŹōŠŌ”¢·Ē½šŹōŠŌµÄĒæČõÅŠ¶Ļ£¬Ö÷ŅŖŹĒĶ¬ÖÜĘŚµŻ±ä¹ęĀÉ”¢½šŹōŠŌ”¢·Ē½šŹōŠŌµÄÅŠ¶ĻŅĄ¾ŻŗĶ·“Ó¦ĻÖĻó±Č½ĻŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®ÕōĘų | B£® | äåÕōĘų | C£® | ČżŃõ»ÆĮņĘųĢå | D£® | Ņ»Ńõ»ÆµŖĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
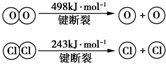 ÓĆCl2Éś²śÄ³Š©ŗ¬ĀČÓŠ»śĪļŹ±»į²śÉśø±²śĪļHCl£®ĄūÓĆ·“Ó¦A£¬æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ£®·“Ó¦A£ŗ4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400”ę}$Cl2+H2O£¬ŅŃÖŖ£ŗ·“Ó¦AÖŠ£¬4mol HCl±»Ńõ»Æ£¬·Å³ö115.6kJµÄČČĮ森
ÓĆCl2Éś²śÄ³Š©ŗ¬ĀČÓŠ»śĪļŹ±»į²śÉśø±²śĪļHCl£®ĄūÓĆ·“Ó¦A£¬æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ£®·“Ó¦A£ŗ4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400”ę}$Cl2+H2O£¬ŅŃÖŖ£ŗ·“Ó¦AÖŠ£¬4mol HCl±»Ńõ»Æ£¬·Å³ö115.6kJµÄČČĮ森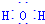 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
| Źµ Ńé ²½ Öč | ½ā ŹĶ »ņ Źµ Ńé ½į ĀŪ |
| £Ø1£©³ĘČ”A 9.0g£¬ÉżĪĀŹ¹ĘäĘū»Æ£¬²āĘäĆܶȏĒĻąĶ¬Ģõ¼žĻĀH2µÄ45±¶£® | ŹŌĶعż¼ĘĖćĢīæÕ£ŗ£Ø1£©AµÄĦ¶ūÖŹĮæĪŖ£ŗ90£® |
| £Ø2£©½«“Ė9.0g AŌŚ×ćĮæ“æO2³ä·ÖČ¼ÉÕ£¬²¢Ź¹Ęä²śĪļŅĄ“Ī»ŗ»ŗĶعżÅØĮņĖį”¢¼īŹÆ»Ņ£¬·¢ĻÖ·Ö±šŌöÖŲ5.4gŗĶ13.2g£® | £Ø2£©AµÄ·Ö×ÓŹ½ĪŖ £ŗC3H6O3£® |
| £Ø3£©ĮķČ”A 9.0g£¬øś×ćĮæµÄNaHCO3·ŪÄ©·“Ó¦£¬Éś³É2.24L CO2£Ø±ź×¼×“æö£©£¬ČōÓė×ćĮ潚ŹōÄĘ·“Ó¦ŌņÉś³É2.24L H2£Ø±ź×¼×“æö£©£® | £Ø3£©AÖŠŗ¬ÓŠ¹ŁÄÜĶŵÄĆū³Ę£ŗ ōČ»ł”¢ōĒ»ł£® |
£Ø4£©AµÄŗĖ“Ź²ÕńĒāĘ×ČēĶ¼£ŗ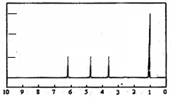 | £Ø4£©AÖŠŗ¬ÓŠ1øöŹÖŠŌĢ¼Ō×Ó£® |
£Ø5£©×ŪÉĻĖłŹö£¬AµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £® £® | |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | v£ØB2£©=4.8 mol/£ØL•min£© | B£® | v£ØA2£©=1.5 mol/£ØL•s£© | ||
| C£® | v£ØC£©=1.6 mol/£ØL•s£© | D£® | v£ØB2£©=1.7 mol/£ØL•s£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ÓŃ¹ | B£® | ¼õŃ¹ | C£® | ½µĪĀ | D£® | ¼õÉŁEµÄÅØ¶Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | PH=1µÄČÜŅŗÖŠ£ŗNa+”¢K+”¢MnO4-”¢CO32- | |
| B£® | ÓÉĖ®µēĄė³öµÄC£ØH+£©=1”Į10-13mol•L-1µÄČÜŅŗÖŠ£ŗMg2+”¢Cu2+”¢SO42-”¢NO3- | |
| C£® | ĪŽÉ«ČÜŅŗÖŠ£ŗCu2+”¢Al3+”¢NH4+”¢Cl- | |
| D£® | 0.1 mol•L-1FeCl3ČÜŅŗÖŠ£ŗFe2+”¢NH4+”¢AlO2-”¢S2- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŹµŃ鱹ŗÅ | ĪĀ¶Č/”ę | H2O2ÅضČ/% | ĘäĖüŹŌ¼Į | ŹµŃéÄæµÄ |
| ¢Ł | 20 | 5 | ĪŽ | £Ø¢ń£©ŹµŃé¢ŁŗĶ¢ŚĢ½¾æ“߻ƼĮ¶ŌH2O2·Ö½āĖŁĀŹµÄÓ°Ļģ£» £Ø¢ņ£©ŹµŃé¢ŚŗĶ¢ŪĢ½¾æĪĀ¶Č¶ŌøĆ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£» £Ø¢ó£©ŹµŃé¢ŚŗĶ¢ÜĢ½¾æH2O2ÅØ¶Č¶ŌøĆ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£® |
| ¢Ś | 20 | 5 | FeCl3 ČÜŅŗ | |
| ¢Ū | ||||
| ¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÓĆ96%µÄ¹¤Ņµ¾Ę¾«ÖĘČ”ĪŽĖ®ŅŅ“¼£¬æɲÉÓƵķ½·ØŹĒ¼ÓÉśŹÆ»Ņ£¬ŌŁÕōĮó | |
| B£® | ŌŚ×é×°ÕōĮó×°ÖĆŹ±£¬ĪĀ¶Č¼ĘµÄĖ®ŅųĒņÓ¦ÉģČėŅŗĆęĻĀ | |
| C£® | ŌŚ±½¼×ĖįÖŲ½į¾§ŹµŃéÖŠ£¬“Ö±½¼×Ėį¼ÓČČČܽāŗó»¹ŅŖ¼ÓÉŁĮæÕōĮóĖ® | |
| D£® | ŌŚ±½¼×ĖįÖŲ½į¾§ŹµŃéÖŠ£¬“ż“Ö±½¼×ĖįĶźČ«ČܽāŗóŅŖĄäČ“µ½³£ĪĀ²Å¹żĀĖ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com