
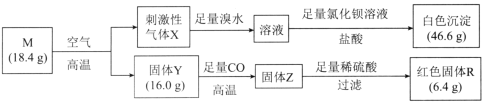
【题目】化合物M由两种位于第四周期的过渡金属元素和一种位于第三周期的非金属元素组成,一定条件下M存在如图所示转化。已知:固体Y中两种金属元素的化合价分别为+2、+3。下列有关推断错误的是( )
A.气体X能使品红溶液、酸性高锰酸钾溶液、含酚酞的碳酸钠溶液褪色
B.溴水吸收气体X的离子方程式为Br2+2H2O+SO22HBr+2H++SO![]()
C.根据上述数据推知,M的化学式为CuFeS2
D.向KNO3和稀盐酸的混合溶液中加入少量固体Z,固体Z全部溶解
【答案】B
【解析】
M在空气中灼烧,产生刺激性气味的气体X,气体X和溴水反应后的溶液与氯化钡反应生成的沉淀是硫酸钡,硫酸钡的物质的量是![]() ,所以M中含有S元素,且物质的量是0.2mol,气体X是二氧化硫;固体Y是金属氧化物,被CO还原为金属Z,红色固体R难溶于硫酸,所以R是Cu,铜的质量是6.4g,固体Y中两种金属元素的化合价分别为+2、+3,则另一种金属为+3价,设另一种金属为T ,氧化物的化学式是
,所以M中含有S元素,且物质的量是0.2mol,气体X是二氧化硫;固体Y是金属氧化物,被CO还原为金属Z,红色固体R难溶于硫酸,所以R是Cu,铜的质量是6.4g,固体Y中两种金属元素的化合价分别为+2、+3,则另一种金属为+3价,设另一种金属为T ,氧化物的化学式是![]() 根据元素守恒,T元素的质量是
根据元素守恒,T元素的质量是![]() ;
;![]() 的质量是
的质量是![]() ,设T元素的相对分子质量是a,则
,设T元素的相对分子质量是a,则![]() ,a=56g/mol,所以T是铁元素。
,a=56g/mol,所以T是铁元素。
A.气体X是二氧化硫,二氧化硫能使品红溶液、酸性高锰酸钾溶液、含酚酞的碳酸钠溶液褪色,故A正确;
B.溴水和二氧化硫反应生成硫酸和氢溴酸,反应的离子方程式为Br2+2H2O+SO2=2Br-+4H++SO![]() ,故B错误;
,故B错误;
C.根据上述数据推知,18.4g M含有Fe元素的物质的量是![]() 、Cu元素的物质的量是
、Cu元素的物质的量是![]() 、S元素的物质的量是0.2mol,M的化学式为CuFeS2,故C正确;
、S元素的物质的量是0.2mol,M的化学式为CuFeS2,故C正确;
D.固体Z是铁、铜的混合物,铁、铜都能溶液稀硝酸,向KNO3和稀盐酸的混合溶液中加入少量固体Z,固体Z全部溶解,故D正确;
选B。


科目:高中化学 来源: 题型:
【题目】随着我国汽车年销量的大幅增加,给空气环境造成了很大的污染。汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )

A. 反应中NO为氧化剂,N2为氧化产物
B. 汽车尾气的主要污染成分包括CO、NO和N2
C. NO和O2必须在催化剂表面才能反应
D. 催化转化总化学方程式为2NO+O2+4CO ![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三草酸合铁酸钾的化学 K3[Fe(C2O4)3]·3H2O 可用于制作工程图中“晒制蓝图”时的感光剂。
(1)钾离子最外层电子的轨道表示式 _________。
(2)已知草酸氢钾(KHC2O4)溶液中c(C2O42—)>c(H2C2O4),则该溶液呈性________(填酸、碱、中),并简述原因_________,写出HC2O4—水解的离子方程式_________________。
为探究三草酸合铁酸钾受热分解的产物,按下图进行实验。
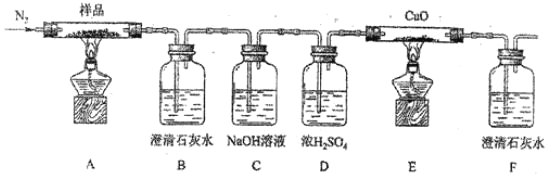
(3)实验开始时,先要通一会氮气,其目的是__________。
(4)实验中观察到装置 B、F 中澄清石灰水均变浑浊,装置 E 中固体变为红色, 由此判断热分解产物中一定含有_________、_________。
(5)样品完全分解后,装置 A 中的残留物含有 FeO 和 Fe2O3,检验 Fe2O3 存在的方法是:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铍(BeO)常温下为不溶于水、易溶于强酸和强碱的固体,除用作耐火材料外,还可以用于制霓虹灯和铍合金。工业上以硅铍石(主要含有BeO、SiO2、MgO,还含有少量Al2O3和Fe2O3)制备高纯度BeO的流程如图所示:
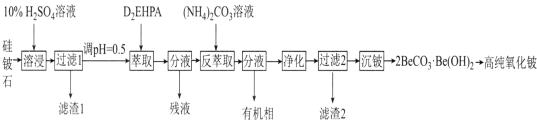
已知:①BeO为离子化合物,熔点为2350℃,BeC12和NaC1等比例混合的固体混合物在350℃即可熔化;
②不同金属阳离子在D2EHPA中的溶解性如下表所示:
Be2+ | Mg2+ | Fe3+ | Al3+ | |
D2EHPA中的溶解性 | 易溶 | 难溶 | 微溶 | 微溶 |
请回答下列问题:
(1)“滤渣1”的主要成分为__(填化学式)。“残液”中含量最多的金属元素为__(填名称)。
(2)“萃取”后铍元素以Be(HX2)2的形式存在于有机相中,“反萃取”后以(NH4)2Be(CO3)2的形式存在于水相中,则“反萃取”时含铍微粒发生反应的化学方程式为___。
(3)“净化”时需将反萃取液加热到70℃,加热到70℃的目的为__。
(4)由2BeCO3·Be(OH)2制备高纯BeO的方法是__。
(5)BeO的电子式为__。工业上常采用电解熔融BeC12与NaC1等比例混合物的方法制备金属Be,不采用电解熔融BeO制备的主要原因为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体中可能含有Na+、K+、Al3+、Ba2+、SO42-、CO32-、SiO32-、等离子,将其配成 100mL 溶液。学生研究性学习小组为了确认其成分,设计并完成了如图所示实验:

请回答下列问题:
(1)配制100mL 溶液需要使用容量瓶,该仪器使用前必须进行的一步操是______________;在“定容”操作中,当液面接近容量瓶刻度线1~2cm 处,改用__________________,再将容量瓶塞盖好,反复上下颠倒,摇匀。
(2)若出现如下情况,导致所配溶液浓度偏高的是_____________________
A.称量时砝码已经生锈;
B.溶解、转移溶液之后没有对烧杯和玻璃棒进行洗涤操作;
C.定容时俯视;
D.定容时,液面超过容量瓶颈上的刻度线,用胶头滴管将过量的液体吸出;
E.容量瓶不干燥,含有少量蒸馏水。
(3) 根据以上实验可得出:一定存在的离子是_________________,,一定不存在的离子是___________________。
(4) 加入稀盐酸,所发生的离子反应方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常利用CO2和NH3合成尿素[CO(NH2)2],该可逆反应分两步进行,整个过程中的能量变化如图所示。下列说法错误的是( )
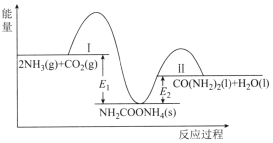
A.NH2COONH4为合成尿素反应的中间产物
B.反应Ⅰ逆反应的活化能>反应Ⅱ正反应的活化能
C.反应Ⅱ在热力学上进行趋势很大
D.2NH3(g)+CO2(g)![]() CO(NH2)2(1)+H2O(1)的焓变△H=El-E2
CO(NH2)2(1)+H2O(1)的焓变△H=El-E2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代的物质文明华夏民族在认识、改造和应用物质方面有着辉煌的历史。
①东晋《抱扑子》中记载:“以曾青涂铁,铁赤色如铜”(“曾青”即硫酸铜溶液)。
②战国《周礼》中记载;“煤饼烧砺房成灰”(“砺房”即牡砺壳,主要成分是碳酸钙)。将“灰”溶于水可制得沤浸树皮脱胶的碱液。
③元代《庚道集》中记载:“点铜戍银”(即单质铜与砷融合形成银白色的物质)
请运用你学过的化学知识回答下列问题;
(1)在①~③中,发生了化学变化的是___(填编号)其中发生分解反应的化学方程式为___。
(2)①中发生变化的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:
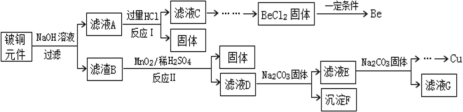
已知:I、铍、铝元素化学性质相似;BeCl2熔融时能微弱电离;
Ⅱ、常温下部分难溶物的溶度积常数如下表:
难溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
溶度积常数(Ksp) | 2.2×10—20 | 4.0×10—38 | 2.1×10—13 |
(1)滤液A的主要成分除NaOH外,还有___________(填化学式),写出反应I中含铍化合物与过量盐酸反应的离子方程式:__________。
(2)①滤液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,最合理的实验步骤顺序为_______(填字母)
a.加入过量的氨水 b.通入过量的CO2 c.加入过量的NaOH d.加入适量的HCl e.洗涤 f.过滤
②从BeCl2溶液中获得BeCl2的晶体易带结晶水,但是将BeCl2晶体与SOCl2(易水解,产物之一能使品红褪色)混合可得无水BeCl2,请从平衡移动角度解释原因:__________。
(3)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅱ中CuS发生反应的化学方程式:______。
(4)滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.0080mol·L-1、c(Mn2+)=0.010mol·L-1,缓慢通氨气调节pH可将其依次分离(体积变化忽略不计)。当Cu2+恰好完全沉淀(c(Cu2+)=1.0×10-5 mol·L-1)时,溶液中c(Cu2+)/ c(Fe3+)约为______。(![]() ≈4.7,保留两位有效数字)
≈4.7,保留两位有效数字)
(5)电解NaCl-BeCl2混合熔盐可制备金属铍。
①电解过程中,加入氯化钠的目的是________。
②电解得到的Be蒸气中约含1%的Na蒸气除去Be中少量Na的方法为________。已知部分物质的熔沸点如下表:
物质 | 熔点(K) | 沸点(K) |
Be | 1551 | 3243 |
Na | 370 | 1156 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2 L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g)pC(g)+qD(g)已知:平均反应速率v(C)=![]() v(A);反应2 min时,A的浓度减少了
v(A);反应2 min时,A的浓度减少了![]() a mol,B的物质的量减少了
a mol,B的物质的量减少了![]() mol,有a mol D生成。
mol,有a mol D生成。
回答下列问题:
(1)反应2 min内,v(A)=________,v(B)=________。
(2)化学方程式中,x=________,y=________,p=________,q=________。
(3)反应平衡时,D为2a mol,则B的转化率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com