



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ں�ˮ�б��ں�ˮ�и���ʴ����Ҫԭ���Ǻ�ˮ���������ں�ˮ |
| B��NaFeO4��������ˮ��ԭ����������Ư�۹�ͬ����ˮ��ԭ����ͬ |
| C�����»��ճ��õ���������ʹH7N9�������в��������ʱ��� |
| D����������������������ЧӦ�������⻯ѧ���������γɶ��뵪�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ����������SO2���壺OH-+SO2=HSO3- |
| B��ϡ�����м���������ۣ�Fe+4H++NO3-=Fe3++NO��+2H2O |
| C����NaOH��Һ���շ����е������NO+NO2+OH-=NO2-+H2O |
| D����̼�������Һ�м�������������������Һ��HCO3-+Ca2++OH-=CaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ũ�����ữ��KMnO4��Һ��H2O2��Ӧ��֤��H2O2���л�ԭ�ԣ�2MnO4-+6H++5H2O2=2Mn2++5O2��+8H2O |
| B������ʯ���ڴ����У�CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2��+H2O |
| C��Mg��HCO3��2��Һ�����NaOH��Mg2++2HCO3-+2OH-=MgCO3��+2H2O+CO32- |
| D����������������Ca2++2ClO-+H2SO3=CaSO3��+2HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
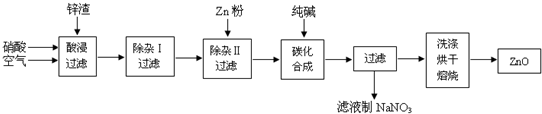
| ������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 | Zn��OH��2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 4 |
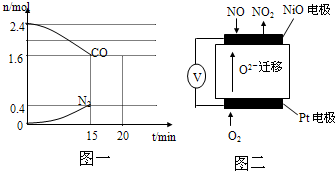
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
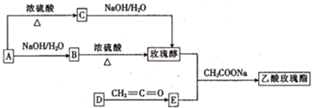
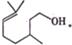

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
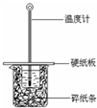 ijʵ��С����0.55mol/L NaOH��Һ��0.50mol/L���ᷴӦ���ⶨ�к��ȣ�ʵ��װ����ͼ��ʾ��
ijʵ��С����0.55mol/L NaOH��Һ��0.50mol/L���ᷴӦ���ⶨ�к��ȣ�ʵ��װ����ͼ��ʾ�� | ��ʼ�¶�t1/�� | ��ֹ�¶� t2/�� | �¶Ȳ�ƽ��ֵ ��t2-t1��/�� | ||
| H2SO4 | NaOH | ƽ��ֵ | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.3 | |
| 2 | 25.9 | 25.9 | 25.9 | 29.0 | |
| 3 | 26.4 | 26.2 | 26.3 | 29.6 | |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com