
| A. | 治理“地沟油”,可通过水解反应制得肥皂 | |
| B. | 硅晶体具有半导体性能,可用于制取光导纤维 | |
| C. | 人类超量碳排放及氮氧化物和二氧化硫的排放是形成酸雨的主要原因 | |
| D. | PM2.5是指空气中直径≤2.5 μm的颗粒物,直径为2.5 μm的颗粒物分散在空气中形成胶体(1μm=10-6m) |
分析 A.地沟油”成分为高级脂肪酸甘油酯,在碱性环境下水解生成高级脂肪酸钠;
B.光导纤维的主要成分为二氧化硅;
C.根据形成酸雨的原因;
D.分散质直径为10-7~10-9m的分散系属于胶体.
解答 解:A.地沟油”成分为高级脂肪酸甘油酯,在碱性环境下水解生成高级脂肪酸钠,可以用来制作肥皂,故A正确;
B.光导纤维的主要成分为二氧化硅,不是晶体硅,故B错误;
C.氮氧化物和二氧化硫的排放是形成酸雨的主要原因,故C错误;
D.胶粒直径为10-7~10-9m的分散系属于胶体,2.55μm的颗粒物直径为2.5×10-6,大于胶体粒子直径,不属于胶体,故D错误;
故选:A.
点评 本题考查了生产、生活中的化学知识,熟悉常见物质的性质是解题关键,题目难度不大.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:填空题
 ,A与B在原子的电子层结构上的相同点是最外层均有4个电子.
,A与B在原子的电子层结构上的相同点是最外层均有4个电子.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述四种氧化物中,至少有三种是碱性氧化物 | |
| B. | 将固体X加入氢氟酸中,X会溶解 | |
| C. | 滤液Y中的阳离子只有Mg2+、Al3+、Fe3+三种 | |
| D. | 滤液Y中加入过量氨水,所得沉淀为Fe(OH)3和Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有④ | B. | 只有⑤ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ①②③ | C. | ①②③⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
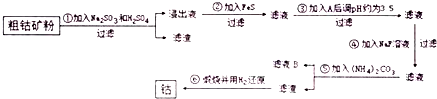
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应后的固体混合物中还含有碳 | |
| B. | 反应后的固体混合物总质量为14.4 g | |
| C. | 反应后的固体混合物中单质Cu的质量为12.8 g | |
| D. | 反应后的固体混合物中氧化物的物质的量为0.05 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com