
| A. | CO2→CO | B. | FeCl2→FeCl3 | C. | HCl→AgCl | D. | KI→I2 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
| 织物 | ① | ② | ③ |
| 灼烧时的气味 | 烧焦羽毛的气味 | 烧纸的气味 | 特殊的气味 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中各离子的浓度都减小 | B. | c(Cl-)/c(NH4+)减小 | ||
| C. | c(H+)/c(NH4+)增大 | D. | c(H+)•c(OH-)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1>△H2 | B. | a=b | C. | a>b | D. | a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe+2HCl═H2↑+FeCl2 | B. | 2FeCl2+Cl2 ═2FeCl3 | ||
| C. | CaO+H2O═Ca(OH)2 | D. | 2Fe(OH)3 $\frac{\underline{\;△\;}}{\;}$Fe2O3+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

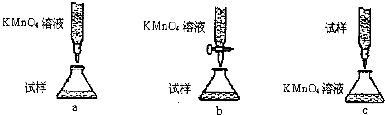
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
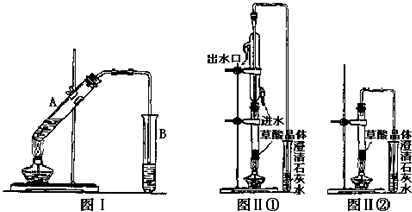
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com