

图7-4
(1)A、C两点的正反应速率的关系为vA_________vC(填“<”“>”或“=”)。
(2)A、B、C、D、正各状态中,v(正)<v(逆)的是_________。
(3)维持p1不变,E→A所需时间为x;维持p2不变,D→C所需时间为y,则x_____________y(填“<”“>”或“=”)。
(4)欲要求使E状态从水平方向到达C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的方法是____________。
A.从p1无限缓慢加压至p2,再由p2无限缓慢降压至p1
B.从p1突然加压至p2,再由p2无限缓慢降压至p1
C.从p1突然加压至p2,再由p2突然降压至p1
D.从p1无限缓慢加压至p2,再由p2突然降压至p1
(1)< (2)D (3)> (4)B
提示:(1)由于C点对应的压强大于A点的压强,所以正反应速率vA<vC。
(2)A、B、C三点都在平衡线上,所以此三点的正逆反应速率相等。D点要达到平衡,必须降低NO2的百分含量,也就是使平衡向逆反应方向移动,从而得出v(正)<v(逆)。E点要达到平衡,必须提高NO2的质量分数,也就是使平衡向正反应方向移动,从而得出v(正)>v(逆)。故答案为D。
(3)AE与DC线段的长度相等,也就是NO2的体积变化量相等。但由于D点的压强大于正点的压强,所以D点的反应速率大于正点的反应速率,故所需时间x>y。
(4)对于压强的改变,当快速加压时,平衡未移动,但压强迅速增大,反映在图像上就是纵坐标不变,横坐标不断增大;当缓慢加压时,平衡不断地被破坏,但又不断地建立新的平衡,所以缓慢加压时,NO2的体积分数的变化应不断地在平衡曲线上滑动。所以“使E状态从水平方向到达C状态”,应突然加压;“由C沿平衡曲线以达A状态”,应缓慢降压。答案为B。


科目:高中化学 来源: 题型:
 对于N2O4(g)
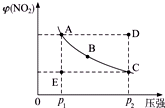
对于N2O4(g) 2NO2(g)在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点).
2NO2(g)在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点).查看答案和解析>>
科目:高中化学 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
对于N2O4(g)![]() 2NO2(g),反应达平衡后,K为平衡常数,保持温度不变.
2NO2(g),反应达平衡后,K为平衡常数,保持温度不变.
(1)压强增大,体积________,浓度________.K变吗?________;Q变吗?________.由于Δv>0,所以Q________K,平衡向________移动.
(2)压强减小,体积________,浓度________.K变吗?________;Q变吗?________.由于Δv>0,所以Q________K,平衡向________移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
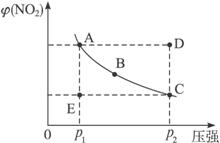
(1)A、C两点的正反应速率的关系为A____________(填“<”“>”或“=”)C。
(2)A、B、C、D、E各状态中,v(正)<v(逆)的是____________________。
(3)维持p1不变,E→A所需时间为x;维持p2不变,D→C所需时间为y,则x________y (填“<”“>”或“=”)。
(4)欲要求使E状态从水平方向到达C状态后,再沿平衡曲线以达A状态,从理论上来讲,可选用的条件是____________________。
A.从p1无限缓慢加压至p2,再由p2无限缓慢降压至p1
B.从p1突然加压至p2,再由p2无限缓慢降压至p1
C.从p1突然加压至p2,再由p2突然降压至p1
D.从p1无限缓慢加压至p2,再由p2突然降压至p1
查看答案和解析>>
科目:高中化学 来源:2011-2012学年上海市闵行区高三上学期期末质量抽测化学试卷 题型:填空题
下图是煤化工产业链的一部分,试运用所学知识,解决下列问题:

(1)已知该产业链中某反应的平衡表达式为:K=
它所对应反应的化学方程式为 。
已知在一定温度下,在同一平衡体系中各反应的平衡常数如下:
C(s)+CO2(g)  2CO(g),K1
2CO(g),K1
CO(g)+H2O(g)  H2(g)+CO2(g),K2
H2(g)+CO2(g),K2
C(s)+H2O(g)  CO(g)+H2(g),K3
CO(g)+H2(g),K3
则K1、K2、K3之间的关系为 。
(2)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g) H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
|
温度/℃ |
400 |
500 |
800 |
|
平衡常数K |
9.94 |
9 |
1 |
该反应的逆反应方向是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时CO的转化率为 。
(3)对于反应N2O4(g) 2NO2(g)-Q(Q>0),在温度
2NO2(g)-Q(Q>0),在温度
为T1、T2时,平衡体系中NO2的体积分数随压强变化
曲线如图所示。下列说法正确的是 。

A.两种不同的温度比较:T1 > T2
B.A、C两点的反应速率:A<C
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法实现
(4)如右图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率,反应原理为:NO(g) + NO2(g) + 2NH3(g)  2N2(g) + 3H2O(g)
2N2(g) + 3H2O(g)

以下说法正确的是(注:脱氮率即氮氧化物转化率)
A.上述反应的正反应为吸热反应
B.相同条件下,改变压强对脱氮率没有影响
C.曲线①、②最高点表示此时平衡转化率最高
D.催化剂①、②分别适合于250℃和450℃左右脱氮
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com