
ΓΨΧβΡΩΓΩpCάύΥΤ”ΎpHΘ§ «÷ΗΦΪœΓ»ή“Κ÷–»ή÷ ≈®Ε»ΒΡΗΚΕ‘ ΐΓΘ≥ΘΈ¬œ¬œρH2CO3»ή“Κ÷–÷πΒΈΒΈΦ”NaOH»ή“ΚΘ§≤βΒΟ»ή“ΚΒΡpC”κpHΙΊœΒ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ® Θ©
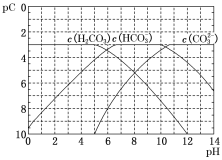
A.‘ΎΆ§“Μ»ή“Κ÷–Θ§H2CO3ΓΔHCO3®CΓΔCO32®C≤ΜΡή¥σΝΩΙ≤¥φ
B.H2CO3ΕΰΦΕΒγάκΤΫΚβ≥Θ ΐKa2ΒΡ ΐΝΩΦΕΒ»”Ύ10®C11
C.Β±pH=7 ±Θ§»ή“Κ÷–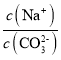 ΘΨ3
ΘΨ3
D.œρH2CO3»ή“ΚΒΈΦ”NaOH»ή“Κ÷Ν»ή“Κ≥ ÷––‘ΒΡΙΐ≥Χ÷–Θ§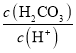 ÷πΫΞ±δ–Γ
÷πΫΞ±δ–Γ
ΓΨ¥πΑΗΓΩD
ΓΨΫβΈωΓΩ
AΘ°H2CO3¥φ‘Ύ”ΎΥα–‘Ϋœ«ΩΒΡ»ή“Κ÷–Θ§CO32-¥φ‘Ύ”ΎΦν–‘Ϋœ«ΩΒΡ»ή“Κ÷–Θ§Υυ“‘‘ΎΆ§“Μ»ή“Κ÷–Θ§H2CO3ΓΔHCO3®CΓΔCO32®C≤ΜΡή¥σΝΩΙ≤¥φΘ§Aœν’ΐ»ΖΘΜ
BΘ°ΫαΚœH2CO3ΒΡΕΰΦΕΒγάκKa2=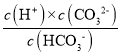 Θ§”…ΆΦœώΩ…÷ΣΘ§Β±c(HCO3-)=c(CO32-)Θ§Ka2Β»”Ύ¥Υ ±»ή“Κ÷–ΒΡc(H+)Θ§”…ΆΦœώ÷ΣpH‘Ύ10ΓΪ11÷°ΦδΘ§Ι H2CO3ΕΰΦΕΒγάκΤΫΚβ≥Θ ΐKa2ΒΡ ΐΝΩΦΕΒ»”Ύ10®C11Θ§Bœν’ΐ»ΖΘΜ
Θ§”…ΆΦœώΩ…÷ΣΘ§Β±c(HCO3-)=c(CO32-)Θ§Ka2Β»”Ύ¥Υ ±»ή“Κ÷–ΒΡc(H+)Θ§”…ΆΦœώ÷ΣpH‘Ύ10ΓΪ11÷°ΦδΘ§Ι H2CO3ΕΰΦΕΒγάκΤΫΚβ≥Θ ΐKa2ΒΡ ΐΝΩΦΕΒ»”Ύ10®C11Θ§Bœν’ΐ»ΖΘΜ
CΘ°Β±pH=7 ±Θ§ΗυΨίΒγΚ… ΊΚψc(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)Θ§Ω…÷Σc(Na+)=c(HCO3-)+2c(CO32-)Θ§”…ΆΦœώΩ…÷ΣΘ§Β±pH=7 ±Θ§»ή“Κ÷–c(CO32-)ΘΦc(HCO3-)Θ§Υυ“‘c(Na+)ΘΨ3c(CO32-)Θ§Φ¥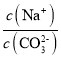 ΘΨ3Θ§Cœν’ΐ»ΖΘΜ
ΘΨ3Θ§Cœν’ΐ»ΖΘΜ
DΘ°H2CO3“ΜΦΕΒγάκΤΫΚβ≥Θ ΐ±μ¥ο ΫKa1=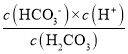 Θ§œρH2CO3»ή“ΚΒΈΦ”NaOH»ή“Κ÷Ν»ή“Κ≥ ÷––‘ΒΡΙΐ≥Χ÷–Θ§c(HCO3-)‘ω¥σΘ§Ka1≤Μ±δΘ§Υυ“‘
Θ§œρH2CO3»ή“ΚΒΈΦ”NaOH»ή“Κ÷Ν»ή“Κ≥ ÷––‘ΒΡΙΐ≥Χ÷–Θ§c(HCO3-)‘ω¥σΘ§Ka1≤Μ±δΘ§Υυ“‘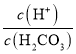 Φθ–ΓΘ§Φ¥
Φθ–ΓΘ§Φ¥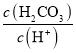 ÷πΫΞ±δ¥σΘ§Dœν¥μΈσΘΜ
÷πΫΞ±δ¥σΘ§Dœν¥μΈσΘΜ
¥πΑΗ―ΓDΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ0.1 molΒΡΟΨΓΔ¬ΝΜλΚœΈο»ή”Ύ100 mL 2molΓΛLΘ≠1H2SO4»ή“Κ÷–Θ§»ΜΚσ‘ΌΒΈΦ”1 molΓΛLΘ≠1NaOH»ή“ΚΓΘ«κΜΊ¥πΘΚ
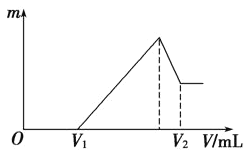
Θ®1Θ©»τ‘ΎΒΈΦ”NaOH»ή“ΚΒΡΙΐ≥Χ÷–Θ§≥ΝΒμ÷ ΝΩmΥφΦ”»κNaOH»ή“ΚΒΡΧεΜΐV±δΜ·»γΆΦΥυ ΨΓΘΒ±V1ΘΫ120mL ±Θ§‘ρΫπ τΖέΡ©÷–n(Mg)ΘΫ________Θ§V2ΘΫ________mLΓΘ
Θ®2Θ©»τ‘ΎΒΈΦ”NaOH»ή“ΚΙΐ≥Χ÷–Θ§”ϊ ΙMg2ΘΪΓΔAl3ΘΪΗ’ΚΟ≥ΝΒμΆξ»ΪΘ§‘ρΒΈ»κNaOH»ή“ΚΒΡΧεΜΐV(NaOH)ΘΫ________mLΓΘ
Θ®3Θ©»τœρ300mL 1 mol/LAL2(SO4)3ΒΡ»ή“Κ÷–÷πΫΞΦ”»κ≈®Ε»ΈΣ1mol/LΒΡ![]() »ή“ΚΘ§»τ≤ζ…ζ2.34ΩΥΑΉ…Ϊ≥ΝΒμΘ§‘ρΦ”»κΒΡNaOH»ή“ΚΒΡΧεΜΐΩ…ΡήΈΣ__________ΚΝ…ΐΓΘ
»ή“ΚΘ§»τ≤ζ…ζ2.34ΩΥΑΉ…Ϊ≥ΝΒμΘ§‘ρΦ”»κΒΡNaOH»ή“ΚΒΡΧεΜΐΩ…ΡήΈΣ__________ΚΝ…ΐΓΘ
Θ®4Θ©»τΜλΚœΈο»‘ΈΣ0.1 molΘ§Τδ÷–MgΖέΒΡΈο÷ ΒΡΝΩΖ÷ ΐΈΣaΘ§”Ο100 mL 2 molΓΛLΘ≠1ΝρΥα»ήΫβ¥ΥΜλΚœΈοΚσΘ§‘ΌΦ”»κ460 mL 1 molΓΛLΘ≠1NaOH»ή“ΚΘ§ΥυΒΟ≥ΝΒμ÷–ΈόAl(OH)3ΓΘ¬ζΉψΧθΦΰΒΡaΒΡ»Γ÷ΒΖΕΈß «________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΨέΚœΝρΥαΧζ «Υ°¥Πάμ÷–÷Ί“ΣΒΡ–θΡΐΦΝΓΘ“‘ΜΤΧζΩσΒΡ…’‘ϋ![]() ÷ς“Σ≥…Ζ÷ΈΣFe2O3ΓΔFeOΓΔSiO2Β»
÷ς“Σ≥…Ζ÷ΈΣFe2O3ΓΔFeOΓΔSiO2Β»![]() ΈΣ‘≠Νœ÷Τ»ΓΨέΚœΝρΥαΧζ(Fe2(OH)x(SO4)(3-
ΈΣ‘≠Νœ÷Τ»ΓΨέΚœΝρΥαΧζ(Fe2(OH)x(SO4)(3-![]() ))ΒΡΙΛ“’Νς≥Χ»γΆΦΥυ ΨΘΚ
))ΒΡΙΛ“’Νς≥Χ»γΆΦΥυ ΨΘΚ
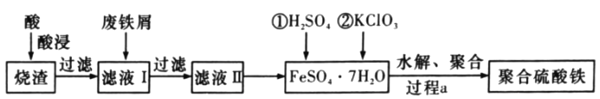
(1)ΓΑΥαΫΰΓ± ±ΉνΚœ ΒΡΥα «______![]() –¥Μ·―ß Ϋ
–¥Μ·―ß Ϋ![]() ΓΘ
ΓΘ
(2)ΓΑΥαΫΰΓ±Κσ»ή“Κ÷–÷ς“ΣΒΡΫπ τ―τάκΉ””–______ΓΘ
(3)Φ”»κKClO3ΒΡΡΩΒΡ «______(ΫαΚœάκΉ”ΖΫ≥Χ ΫΥΒΟς)ΓΘ
(4)ΓΑΙΐ≥ΧaΓ±÷–…ζ≥…ΨέΚœΝρΥαΧζΒΡΙΐ≥Χ «œ»Υ°Ϋβ‘ΌΨέΚœΘ§ΫΪœ¬Ν–Υ°ΫβΖ¥”Π‘≠άμΒΡΜ·―ßΖΫ≥Χ Ϋ≤Ι≥δΆξ’ϊΓΘFe2(SO4)3+______H2O![]() ______Fe2(OH)x(SO4)(3-
______Fe2(OH)x(SO4)(3-![]() )+______ΓΘ
)+______ΓΘ
(5)―ΈΜυΕ»B «ΚβΝΩ–θΡΐΦΝ–θΡΐ–ßΙϊΒΡ÷Ί“Σ÷Η±ξΘ§Ά®≥Θ―ΈΜυΕ»‘ΫΗΏΘ§–θΡΐ–ßΙϊ‘ΫΚΟΓΘ“―÷Σ―ΈΜυΕ»BΒΡ±μ¥ο ΫΈΣB=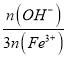 ΓΝ100%(nΈΣΈο÷ ΒΡΝΩ
ΓΝ100%(nΈΣΈο÷ ΒΡΝΩ![]() ΓΘΈΣ≤β≥ωΨέΚœΝρΥαΧζΒΡ―ΈΜυΕ»Θ§Ϋχ––»γœ¬ Β―ι≤ΌΉςΘΚ
ΓΘΈΣ≤β≥ωΨέΚœΝρΥαΧζΒΡ―ΈΜυΕ»Θ§Ϋχ––»γœ¬ Β―ι≤ΌΉςΘΚ
![]() »ΓΨέΚœΝρΥαΧζ―υΤΖmgΘ§Φ”»κΙΐΝΩ―ΈΥαΘ§≥δΖ÷Ζ¥”ΠΘ§‘ΌΦ”»κ÷σΖ–Κσά以ΒΡ’τΝσΥ°Θ§‘ΌΦ”»κKF»ή“ΚΤΝ±ΈFe3+Θ§ ΙFe3+≤Μ”κOH-Ζ¥”ΠΘ§»ΜΚσ“‘Ζ”ΧΣΈΣ÷Η ΨΦΝΘ§”Οcmol/LΒΡ±ξΉΦNaOH»ή“ΚΫχ––÷–ΚΆΒΈΕ®Θ§ΒΫ÷’Βψ ±œϊΚΡNaOH»ή“ΚV0mLΓΘ
»ΓΨέΚœΝρΥαΧζ―υΤΖmgΘ§Φ”»κΙΐΝΩ―ΈΥαΘ§≥δΖ÷Ζ¥”ΠΘ§‘ΌΦ”»κ÷σΖ–Κσά以ΒΡ’τΝσΥ°Θ§‘ΌΦ”»κKF»ή“ΚΤΝ±ΈFe3+Θ§ ΙFe3+≤Μ”κOH-Ζ¥”ΠΘ§»ΜΚσ“‘Ζ”ΧΣΈΣ÷Η ΨΦΝΘ§”Οcmol/LΒΡ±ξΉΦNaOH»ή“ΚΫχ––÷–ΚΆΒΈΕ®Θ§ΒΫ÷’Βψ ±œϊΚΡNaOH»ή“ΚV0mLΓΘ
![]() ΉωΩ’ΑΉΕ‘±» Β―ιΘΚ»Γ”κ≤Ϋ÷ηiΒ»ΧεΜΐΒ»≈®Ε»ΒΡ―ΈΥαΘ§“‘Ζ”ΧΣΈΣ÷Η ΨΦΝΘ§”Οcmol/LΒΡ±ξΉΦNaOH»ή“ΚΫχ––÷–ΚΆΒΈΕ®Θ§ΒΫ÷’Βψ ±œϊΚΡNaOH»ή“ΚVmLΓΘ
ΉωΩ’ΑΉΕ‘±» Β―ιΘΚ»Γ”κ≤Ϋ÷ηiΒ»ΧεΜΐΒ»≈®Ε»ΒΡ―ΈΥαΘ§“‘Ζ”ΧΣΈΣ÷Η ΨΦΝΘ§”Οcmol/LΒΡ±ξΉΦNaOH»ή“ΚΫχ––÷–ΚΆΒΈΕ®Θ§ΒΫ÷’Βψ ±œϊΚΡNaOH»ή“ΚVmLΓΘ
ΔΌΗΟΨέΚœΝρΥαΧζ―υΤΖ÷–Θ§n(OH-)=______molΓΘ
ΔΎ“―÷ΣΗΟ―υΤΖ÷–FeΒΡ÷ ΝΩΖ÷ ΐΈΣ![]() Θ§‘ρ―ΈΜυΕ»B=______ΓΘ
Θ§‘ρ―ΈΜυΕ»B=______ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Ά≠νήΩσ ·÷ς“ΣΚ§”–CoO(OH)ΓΔCoCO3ΓΔCu2(OH)2CO3ΚΆSiO2Θ§ΦΑ“ΜΕ®ΝΩΒΡFe2O3ΓΔMgOΚΆCaOΒ»ΓΘ”…ΗΟΩσ ·÷ΤCo2O3ΒΡ≤ΩΖ÷ΙΛ“’Νς≥Χ»γœ¬ΘΚ
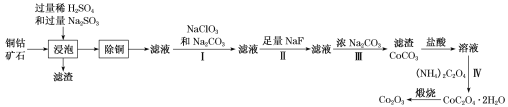
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©ΓΑΫΰ≈ίΓ±Ιΐ≥Χ÷–Θ§νή(III)Ω…ΉΣΜ·ΈΣCoSO4Θ§–¥≥ωΗΟΉΣΜ·ΒΡΜ·―ßΖΫ≥Χ ΫΘΚ________ΓΘ
Θ®2Θ©ΓΑ≥ΐΆ≠Γ±»τ―Γ”ΟMnSΘ§ΦΤΥψ≥ΘΈ¬œ¬ΗΟΓΑ≥ΐΆ≠Γ±Ζ¥”ΠΒΡΤΫΚβ≥Θ ΐK=________ΓΘΘέ±ΘΝτ2ΈΜ”––ß ΐΉ÷ΘΜ“―÷Σ≥ΘΈ¬œ¬Ksp(MnS)=2.5ΓΝ10®C13Θ§Ksp(CuS)=1.3ΓΝ10®C36]
Θ®3Θ©ΔΌ≤Ϋ÷ηI÷–Φ”»κNaClO3Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_______ΓΘ
ΔΎ≥ΘΈ¬œ¬Θ§»ή“Κ÷–Ϋπ τάκΉ”(Mn+)ΒΡpMΘέpM=®Clgc(Mn+)]Υφ»ή“ΚpH±δΜ·ΙΊœΒ»γΆΦΥυ ΨΘ§…ηΦ”»κNaClO3ΚσΘ§»ή“Κ÷–ΒΡc(CO2+)ΈΣ0.1molL®C1Θ§“άΨί»γΆΦΖ÷ΈωΘ§≤Ϋ÷ηI÷–Φ”»κNa2CO3Βς’ϊ»ή“ΚpHΖΕΈßΈΣ_____ΓΘΘέΒ±c(Mn+)Γή10®C6 molL®C1Θ§Φ¥»œΈΣΗΟΫπ τάκΉ”≥ΝΒμΆξ»Ϊ]

Θ®4Θ©≤Ϋ÷ηII÷–Φ”»κΉψΝΩNaFΒΡΡΩΒΡ «________ΓΘ
Θ®5Θ©Ιΐ¬Υ≥ωΒΡCoC2O42H2OΙΧΧεΨ≠œ¥Β”ΚσΘ§÷ΛΟςΙΧΧε“―œ¥ΨΜΒΡ≤ΌΉςΈΣ________ΓΘ
Θ®6Θ©»τΡ≥ΙΛ≥ß”Οm1kgΗΟΆ≠νήΩσ ·÷Τ±ΗΝΥm2kgCo2O3Θ§ΦΌ…η≤ζ¬ ΈΣaΘ§‘ρΗΟΩσ ·÷–νή‘ΣΥΊΒΡΑΌΖ÷Κ§ΝΩΈΣ________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥τ―θ «άμœκΒΡ―ΧΤχΆ―œθ ‘ΦΝΘ§ΤδΆ―œθΖ¥”ΠΈΣΘΚ2NO2(g)ΘΪO3(g) ![]() N2O5(g)ΘΪO2(g)Θ§»τΖ¥”Π‘ΎΚψ»ίΟή±’»ίΤς÷–Ϋχ––Θ§œ¬Ν–”…ΗΟΖ¥”ΠœύΙΊΆΦœώΉς≥ωΒΡ≈–Εœ’ΐ»ΖΒΡ «(ΓΓΓΓ)
N2O5(g)ΘΪO2(g)Θ§»τΖ¥”Π‘ΎΚψ»ίΟή±’»ίΤς÷–Ϋχ––Θ§œ¬Ν–”…ΗΟΖ¥”ΠœύΙΊΆΦœώΉς≥ωΒΡ≈–Εœ’ΐ»ΖΒΡ «(ΓΓΓΓ)
A | B | C | D |
|
|
|
|
…ΐΗΏΈ¬Ε»Θ§ΤΫΚβ≥Θ ΐΦθ–Γ | 0ΓΪ3 sΡΎΘ§Ζ¥”ΠΥΌ¬ ΈΣΘΚv(NO2)ΘΫ0Θ°2 molΓΛLΘ≠1 | t1 ±ΫωΦ”»κ¥ΏΜ·ΦΝΘ§ΤΫΚβ’ΐœρ“ΤΕ· | ¥οΤΫΚβ ±Θ§ΫωΗΡ±δxΘ§‘ρxΈΣc(O2) |
A. AB. BC. CD. D
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕ‘”ΎΩ…ΡφΖ¥”Π4NH3(g)ΘΪ5O2(g) ![]() 4NO(g)ΘΪ6H2O(g)Θ§œ¬Ν––π ω’ΐ»ΖΒΡ «(ΓΓΓΓ)
4NO(g)ΘΪ6H2O(g)Θ§œ¬Ν––π ω’ΐ»ΖΒΡ «(ΓΓΓΓ)
A. Μ·―ßΤΫΚβ≥Θ ΐΒΡ±μ¥ο ΫKΘΫ![]()
B. Β±v’ΐ(NH3)ΓΟv’ΐ(NO)ΘΫ1ΓΟ1 ±Θ§ΥΒΟςΗΟΜ·―ßΖ¥”Π“―Ψ≠¥οΒΫΤΫΚβΉ¥Χ§
C. »τ¥οΒΫΤΫΚβΉ¥Χ§ ±ΝΫ÷÷Ζ¥”ΠΈοΒΡΉΣΜ·¬ œύΒ»Θ§‘ρΤπ ΦΆΕ»κ ±n(NH3)ΓΟn(O2)ΘΫ5ΓΟ4
D. Ζ¥”Π¥οΒΫΤΫΚβΉ¥Χ§ΚσΘ§Κψ»ίΧθΦΰœ¬÷ΜΒςΫΎNH3ΚΆNOΒΡΝΩΘ§Ω…±Θ≥÷‘≠ΤΫΚβΉ¥Χ§
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΗθΒΡΜ·ΚœΈο‘Ύ“Ϋ“©ΓΔ≤ΡΝœΝλ”ρ”–÷Ί“ΣΉς”ΟΘ§»œ ΕΗθΦΑΤδΜ·ΚœΈο”–÷Ί“Σ“β“εΓΘ
Θ®1Θ©ΜυΧ§Ηθ‘≠Ή”÷–Θ§ΒγΉ”’ΦΨίΒΡΉνΗΏΡήΦΕΖϊΚ≈ΈΣ_____________ΓΘ
Θ®2Θ©―–ΨΩ±μΟςΘ§Β±Μ·ΚœΈοΒΡ―τάκΉ””–Έ¥≥…Ε‘ΒγΉ” ±Θ§ΗΟΜ·ΚœΈοΨΏ”–¥≈–‘ΓΘœ¬Ν–Έο÷ Ω…”ΟΉς¬Φ“τ¥χ¥≈ΖέΒΡ «__________ΓΘ
AΘ°V2O5 BΘ°Fe2O3 CΘ°ZnO DΘ°CrO2
Θ®3Θ©“―÷ΣCr3+‘ΎΥ°»ή“Κ÷–ΒΡ¥φ‘Ύ–Έ ΫΈΣ[Cr(H2O)6Θί3+ΓΘ‘Ύ≤ΜΆ§ΧθΦΰœ¬Θ§Ω…¥”CrCl3Υ°»ή“Κ÷–ΜώΒΟΉœ…ΪΓΔάΕ¬Χ…ΪΜρ¬Χ…ΪΒ»≤ΜΆ§―’…ΪΒΡ≈δΚœΈοΘ§Τδ Β―ι ΫΨυΈΣCrCl36H2OΓΘœ÷»ΓάΕ¬Χ…Ϊ≈δΚœΈο0.1molΘ§Φ”»κΉψΝΩAgNO3»ή“ΚΘ§Ψ≠Ιΐ¬ΥΓΔœ¥Β”ΓΔΗ…‘οΒΟ28.7g≥ΝΒμΘ§‘ρΗΟΜ·ΚœΈο÷–ΒΡΜ·―ßΦϋάύ–Ά”–___________Θ§–¥≥ωΗΟάΕ¬Χ…Ϊ≈δΚœΈοΒΡΒγάκΖΫ≥Χ ΫΘΚ________ΓΘ
Θ®4Θ©≥ΘΈ¬œ¬Θ§¬»Μ·θΘΗθ(CrO2Cl2) «ΑΒΚλ…Ϊ“ΚΧεΘ§Ρή”κCCl4ΓΔCS2Β»”–Μζ»ήΦΝΜΞ»ήΓΘ
ΔΌΙΧΧ嬻̷θΘΗθ τ”Ύ______Θ®ΧνΓΑΦΪ–‘Γ±ΜρΓΑΖ«ΦΪ–‘Γ±Θ©Ζ÷Ή”Θ§≈–Εœ“άΨί «______ΓΘ
ΔΎΒ»ΒγΉ”Χε «ΨΏ”–œύΆ§ΒΡΦέΒγΉ” ΐΚΆ‘≠Ή” ΐΒΡΖ÷Ή”ΜράκΉ”ΓΘ–¥≥ω“Μ÷÷”κCCl4Ζ÷Ή”ΜΞΈΣΒ»ΒγΉ”ΧεΒΡ“θάκΉ”ΘΚ_______Θ®ΧνΜ·―ß ΫΘ©ΘΜ–¥≥ωCS2Ζ÷Ή”ΒΡΒγΉ” ΫΘΚ____________ΓΘ
Θ®5Θ©ΒΣΜ·Ηθ(CrN)‘Ύ≥§ΦΕΒγ»ίΤςΝλ”ρ”–ΝΦΚΟ”Π”Ο«ΑΨΑΘ§ΤδΨßΧεΫαΙΙάύ–Ά”ꬻ̷ΡΤœύΆ§ΓΘ
ΔΌΒΣΜ·ΗθΒΡ»έΒψ±»¬»Μ·ΡΤΗΏΒΡ÷ς“Σ‘≠“ρ «______ΓΘ
ΔΎ”κCr3+¥ΈΝΎΫϋΒΡN3®C”–________ΗωΓΘ
Δέ“―÷ΣCr3+ΚΆN3®CΑκΨΕΖ÷±πΈΣapmΓΔbpmΘ§…ηCr3+ΚΆN3®CΕΦ «ΫτΟήΫ”¥ΞΒΡΗ’–‘–Γ«ρΘ§NA¥ζ±μΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΘ§ΨßΧεΒΡΟήΕ»ΈΣΠ―gcm®C3Θ§‘ρCrNΒΡΡΠΕϊ÷ ΝΩΈΣ______ΓΘΘ®”ΟΚ§aΓΔbΓΔNAΓΔΠ―ΒΡΥψ Ϋ±μ ΨΘ©
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥―–ΨΩ–ΓΉιœρΡ≥2 LΟή±’»ίΤς÷–Φ”»κ“ΜΕ®ΝΩΒΡΙΧΧεAΚΆΤχΧεBΘ§ΖΔ…ζΖ¥”ΠA(s)ΘΪ2B(g)![]() D(g)ΘΪE(g)ΓΓΠΛHΘΫQ kJΓΛmolΘ≠1ΓΘ‘ΎTΓφ ±Θ§Ζ¥”ΠΫχ––ΒΫ≤ΜΆ§ ±Φδ≤βΒΟΗςΈο÷ ΒΡΈο÷ ΒΡΝΩ»γ±μΘΚ
D(g)ΘΪE(g)ΓΓΠΛHΘΫQ kJΓΛmolΘ≠1ΓΘ‘ΎTΓφ ±Θ§Ζ¥”ΠΫχ––ΒΫ≤ΜΆ§ ±Φδ≤βΒΟΗςΈο÷ ΒΡΈο÷ ΒΡΝΩ»γ±μΘΚ
ΓΓΓΓΓΓ ±Φδ(min) Έο÷ ΒΡΝΩ(mol)ΓΓΓΓΓΓΓΓΓΓ | 0 | 10 | 20 | 30 | 40 | 50 |
B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
(1)TΓφ ±Θ§ΗΟΖ¥”ΠΒΡΤΫΚβ≥Θ ΐKΘΫ________ΓΘ
(2)30minΚσΘ§÷ΜΗΡ±δΡ≥“ΜΧθΦΰΘ§Ζ¥”Π÷Ί–¬¥οΒΫΤΫΚβΘ§ΗυΨί±μ÷–ΒΡ ΐΨί≈–ΕœΗΡ±δΒΡΧθΦΰΩ…Ρή «________(ΧνΉ÷ΡΗ±ύΚ≈)ΓΘ
aΘ°Ά®»κ“ΜΕ®ΝΩΒΡB bΘ°Φ”»κ“ΜΕ®ΝΩΒΡΙΧΧεA cΘ° Β±Υθ–Γ»ίΤςΒΡΧεΜΐ dΘ°…ΐΗΏΖ¥”ΠΧεœΒΈ¬Ε» eΘ°Ά§ ±Φ”»κ0.2mol BΓΔ0.1mol DΓΔ0.1mol E
(3)–¥≥ωœ¬Ν–ΒγΫβ÷ ‘ΎΥ°÷–ΒΡΒγάκΖΫ≥Χ ΫΘΚ
CH3COOHΘΚ____________NaHSO4ΘΚ______ NaHCO3ΘΚ_________H2CO3ΘΚ_________
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΐΝρΥαΡΤ(Na2S2O8)ΨΏ”–ΦΪ«ΩΒΡ―θΜ·–‘Θ§«“≤ΜΈ»Ε®Θ§Ρ≥Μ·―ß–Υ»Λ–ΓΉιΧΫΨΩΙΐΝρΥαΡΤΒΡœύΙΊ–‘÷ Θ§ Β―ι»γœ¬ΓΘ“―÷ΣSO3 «Έό…Ϊ“ΉΜ”ΖΔΒΡΙΧΧεΘ§»έΒψ16.8ΓφΘ§Ζ–Βψ44.8ΓφΓΘ
Θ®1Θ©Έ»Ε®–‘ΧΫΨΩ(ΉΑ÷Ο»γΆΦ)ΘΚ
Ζ÷Ϋβ‘≠άμΘΚ2Na2S2O8![]() 2Na2SO4ΘΪ2SO3ΓϋΘΪO2ΓϋΓΘ
2Na2SO4ΘΪ2SO3ΓϋΘΪO2ΓϋΓΘ
¥ΥΉΑ÷Ο”–Οςœ‘¥μΈσ÷°¥ΠΘ§«κΗΡ’ΐΘΚ______________________Θ§Υ°≤έ±υΥ°‘ΓΒΡΡΩΒΡ «____________________ΘΜ¥χΜπ–«ΒΡΡΨΧθΒΡœ÷œσ_______________ΓΘ
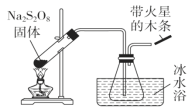
Θ®2Θ©ΙΐΝρΥαΡΤ‘ΎΥα–‘ΜΖΨ≥œ¬Θ§‘ΎAgΘΪΒΡ¥ΏΜ·Ής”Οœ¬Ω…“‘Α―Mn2ΘΪ―θΜ·ΈΣΉœΚλ…ΪΒΡάκΉ”Θ§ΥυΒΟ»ή“ΚΦ”»κBaCl2Ω…“‘≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§ΗΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ______________________Θ§ΗΟΖ¥”ΠΒΡ―θΜ·ΦΝ «______________Θ§―θΜ·≤ζΈο «________ΓΘ
Θ®3Θ©œρ…œ ω»ή“Κ÷–Φ”»κΉψΝΩΒΡBaCl2Θ§Ιΐ¬ΥΚσΕ‘≥ΝΒμΫχ––œ¥Β”ΒΡ≤ΌΉς «___________________________ΓΘ
Θ®4Θ©Ω…”ΟH2C2O4»ή“ΚΒΈΕ®≤ζ…ζΒΡΉœΚλ…ΪάκΉ”Θ§»Γ20mL¥ΐ≤β“ΚΘ§œϊΚΡ0.1molΓΛLΘ≠1ΒΡH2C2O4»ή“Κ30mLΘ§‘ρ…œ ω»ή“Κ÷–ΉœΚλ…ΪάκΉ”ΒΡ≈®Ε»ΈΣ______molΓΛLΘ≠1Θ§»τNa2S2O8”– Θ”ύΘ§‘ρ≤βΒΟΒΡΉœΚλ…ΪάκΉ”≈®Ε»ΫΪ________(ΧνΓΑΤΪΗΏΓ±ΓΑΤΪΒΆΓ±ΜρΓΑ≤Μ±δΓ±)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com