
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 |  | 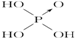 |  |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 ,亚砷酸
,亚砷酸 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由Cl2+2KBr═2KCl+Br2所以F2也能与KBr溶液反应置换出Br2 | |
| B. | 常温下,由Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,所以Fe也能与浓硝酸反应产生NO2 | |
| C. | 由Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2 所以Cu+I2$\frac{\underline{\;\;△\;\;}}{\;}$CuI2 | |
| D. | 由钠保存在煤油中,所以钾也可以保存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Na2O2与水反应,转移电子1mol | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应的产物也相同 | |
| C. | 钠能与氧气和水反应,钠暴露在空气中最终的产物是NaOH | |
| D. | 将0.01mol的Na2O和Na2O2分别投入同质量的水中,所得到的溶质质量分数不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 同位素 | 同位素的质量分数 | 原子百分比 |
| 103A | 103 | 20% |
| 105A | 105 | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
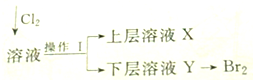 实验室用含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的溶液进行有关实验.已知:Cl2+2Br-=Br2+2Cl-.
实验室用含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的溶液进行有关实验.已知:Cl2+2Br-=Br2+2Cl-.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com