

| A. | 储存液溴 | B. | 提纯含少量水的乙醇 | ||
| C. | 分离CCl4和水 | D. | 吸收氨气 |
分析 A.溴易挥发,且溶于橡胶;
B.提纯含少量水的乙醇,加CaO与水反应后增大与乙醇的沸点差异,然后蒸馏;
C.分离CCl4和水,水在上层,先分离出下层液体;
D.氨气极易溶于水.
解答 解:A.溴易挥发,且溶于橡胶,则不能使用胶头滴管密封,故A错误;
B.提纯含少量水的乙醇,加CaO与水反应后增大与乙醇的沸点差异,然后蒸馏,则图中蒸馏装置合理,故B正确;
C.分离CCl4和水,水在上层,先分离出下层液体,再分离上层液体,故C错误;
D.氨气极易溶于水,图中装置可发生倒吸,故D错误;
故选B.
点评 本题考查化学实验方案的评价及实验装置的综合应用,为高频考点,把握物质的性质、装置的作用、实验技能为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验方案 | 实验目的或结论 |
| A | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 可证明氧化性:H2O2比Fe3+强 |
| B | 向1mL 1%的NaOH溶液中加入2mL 2%的CuSO4溶液,振荡,再加入0.5mL有机物Y,加热,未出现砖红色沉淀 | 说明Y中不含醛基 |
| C[ | 将一定量的NaNO3和KCl的混合液加热并 浓缩至有晶体析出时,趁热过滤 | 得到NaCl晶体 |
| D | 比较不同反应的反应热数据大小 | 从而判断反应速率的大小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ①②③ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
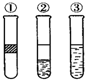 在盛有溴水的三支试管中分别加入苯、四氯化碳和酒精,振荡后静置,出现如图所示现象,则加入的试剂分别是( )
在盛有溴水的三支试管中分别加入苯、四氯化碳和酒精,振荡后静置,出现如图所示现象,则加入的试剂分别是( )| A. | ①是苯,②是CCl4,③是酒精 | B. | ①是酒精,②是CCl4,③是苯 | ||
| C. | ①是CCl4,②是苯,③是酒精 | D. | ①是苯,②是酒精,③是CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
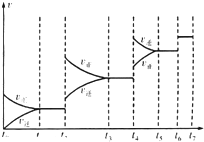 对碳硫及其化合物的研究有重要的意义.
对碳硫及其化合物的研究有重要的意义.| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | X | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | Y | t |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、D、E、G、L、M是核电荷数依次增大的6种短周期主族元素,其中A的原子序数与周期序数相等,D、G、L、M基态原子的最外能层均有2个未成对电子.R+核外有28个电子.请回答下列问题(用所对应的元素符号表示).
已知A、D、E、G、L、M是核电荷数依次增大的6种短周期主族元素,其中A的原子序数与周期序数相等,D、G、L、M基态原子的最外能层均有2个未成对电子.R+核外有28个电子.请回答下列问题(用所对应的元素符号表示).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
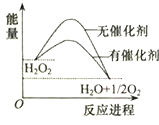
| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热化学方程式:H2O2→H2O+$\frac{1}{2}$O2+Q | |
| D. | 反应物的总能量高于生成物的总能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com