
| A、体积都是22.4L |
| B、具有相同的体积 |
| C、具有相同的原子数 |
| D、具有相同的分子数 |


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
| A、摩尔是国际科学界建议采用的一种物理量 |
| B、2H既可表示2个氢原子又可表示2 mol氢分子 |
| C、1mol氧含6.02×1023个O2 |
| D、摩尔是物质的量的单位,简称摩,符号为mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3 溶液中投入过量Na:Al3++4Na+2H2O═AlO2-+4Na++2H2↑ |
| B、苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- |
| C、硫化钠的水解反应:S2-+H2O?HS-+OH- |
| D、NaClO 溶液中通入过量SO2:ClO-+SO2+H2O═HClO+HS03- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,22.4LCO2中含有NA个CO2分子 |
| B、1.7 gH2O2中含有电子数为0.9NA |
| C、标准状况下,2.24LH2O含有的分子数等于0.1NA |
| D、分子总数为NA的CO和C2H4混合气体体积约为22.4L则质量为28g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同种胶体带同种电荷,相互排斥,是胶体稳定的主要原因 |
| B、生石灰与水混合的过程只发生物理变化 |
| C、O3是由3个氧原子构成的化合物 |
| D、可用丁达尔效应区分溶液与胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
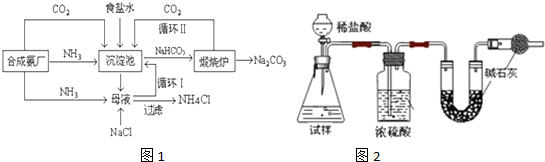
| 盐 | NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3?10H2O |
| 10℃ | 35.8 | 33.3 | 8.1 | 15.8 | 12.5 |
| 20℃ | 36.0 | 37.2 | 9.6 | 21 | 21.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com