
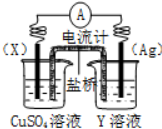
 如图蓄电池是一种可以反复充电、放电的装置.有一种蓄电池在充电和放电时发生的反应是:NiO2+Fe+2H2O$?_{充电}^{放电}$Fe(OH)2+Ni(OH)2
如图蓄电池是一种可以反复充电、放电的装置.有一种蓄电池在充电和放电时发生的反应是:NiO2+Fe+2H2O$?_{充电}^{放电}$Fe(OH)2+Ni(OH)2分析 蓄电池在充电和放电时发生的反应是:NiO2+Fe+2H2O$?_{充电}^{放电}$Fe(OH)2+Ni(OH)2,放电时原电池反应负极反应为:Fe-2e-+2OH-=Fe(OH)2,原电池的正极为:NiO2+2e-+2H2O=Ni(OH)2+2OH-;据此分析.
解答 解:①原电池的正极为:NiO2+2e-+2H2O=Ni(OH)2+2OH-,则NiO2得电子发生还原反应,A选项符合,
故答案为:A;
②该电池放电时,原电池的正极为:NiO2+2e-+2H2O=Ni(OH)2+2OH-,溶液中氢氧根离子难度增大,所以正极附近溶液的pH增大;
故答案为:增大;
③原电池的正极为:NiO2+2e-+2H2O=Ni(OH)2+2OH-;
故答案为:NiO2+2e-+2H2O=Ni(OH)2+2OH-.
点评 本题考查了原电池、电解池原理的分析判断和应用,注意根据电池总反应中元素的化合价的变化判断,注意电极方程式的书写方法,题目难度中等,侧重于学生的分析能力的考查.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 加热胆矾失去结晶水的过程称风化 | |
| B. | 在饱和溶液中,溶质溶解的速率等于结晶速率 | |
| C. | 原电池是把电能转化为化学能的装置 | |
| D. | 电能是二次能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
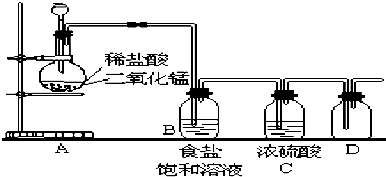
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 精炼铜时粗铜做阴极,纯铜做阳极 | |
| B. | 电解MgCl2饱和溶液,可制得金属镁 | |
| C. | 钢铁的腐蚀通常为电化学腐蚀,该腐蚀过程中负极反应为:Fe-3e-═Fe3+ | |
| D. | 氯碱工业和金属钠的冶炼都用到了NaCl,阳极反应都是:2Cl--2e-═Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油、煤、天然气、油脂都属于化石燃料 | |
| B. | 油脂在碱性条件下的水解反应又称为皂化反应 | |
| C. | 分子式为(C6H10O5)n的淀粉和纤维素互为同分异构 | |
| D. | 蔗糖是还原性糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由ZR组成的化合物为离子化合物 | B. | 含氧酸酸性R>X | ||
| C. | X、Y只能共存于共价化合物中 | D. | 原子半径Z>R>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17g NH3所含的电子数是 10NA | |
| B. | 常温常压下,22.4L氧气含氧原子数为2NA | |
| C. | 5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA | |
| D. | 2.3g金属钠全部变成钠离子时失去的电子数是0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| B. | 用氯化铁溶液腐蚀铜板:Fe3++Cu═Cu2++Fe2+ | |
| C. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | Fe3O4与足量稀HNO3反应:3Fe3O4+28H++NO3-═9Fe3++NO↑+14H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑥⑦ | B. | ①②⑤⑦⑧ | C. | ②③④⑤⑥ | D. | ①③⑥⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com