
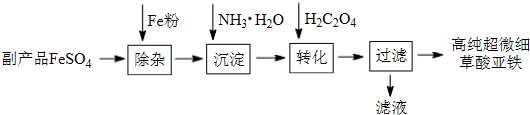
分析 副产品FeSO4(含Al(SO4)3和少量重金属离子)中加入铁粉,将少量重金属离子等除去,得到比较纯净的FeSO4溶液,向FeSO4溶液中加入氨水,生成氢氧化亚铁,氢氧化亚铁和草酸反应生成高纯超微细草酸亚铁沉淀;
(1)温度不宜过高的原因除了控制沉淀的粒径外,还有NH3•H2O受热易分解,挥发出NH3,Fe(OH)2受热易分解;
(2)沉淀前的溶液中含有硫酸亚铁,沉淀步骤中加入一水合氨,生成氢氧化亚铁沉淀和硫酸铵;
(3)多步反应找关系式;
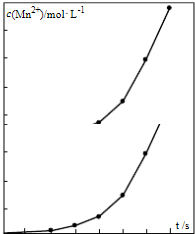
(4)观察图象分析反应速率变大的因素.
解答 解:副产品FeSO4(含Al(SO4)3和少量重金属离子)中加入铁粉,将少量重金属离子等除去,得到比较纯净的FeSO4溶液,向FeSO4溶液中加入氨水,生成氢氧化亚铁,氢氧化亚铁和草酸反应生成高纯超微细草酸亚铁沉淀;
(1)沉淀过程为一水合氨沉淀亚铁离子的过程,生成氢氧化亚铁,氢氧化亚铁不稳定,受热会分解,另外一水合氨受热也会分解,故反应温度不能太高,所以温度不宜过高的原因除了控制沉淀的粒径外,还有NH3•H2O受热易分解,挥发出NH3,Fe(OH)2受热易分解;
故答案为:NH3•H2O受热易分解,挥发出NH3,Fe(OH)2受热也易分解;
(2)沉淀前的溶液中含有硫酸亚铁,沉淀步骤中加入一水合氨,生成氢氧化亚铁沉淀和硫酸铵,所以副产品含有是(NH4)2SO4;
故答案为:(NH4)2SO4;
(3)由题意知氧化C2O42-和Fe2+共消耗0.2000 mol•L-1标准KMnO4溶液体积30.40 mL,步骤3、4标准KMnO4溶液只氧化Fe2+消耗KMnO4溶液体积10.00mL,所以C2O42-消耗KMnO4溶液体积为(30.40-10.00)=20.4mL,由5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O得5C2O42-~2MnO4-,所以n(C2O42-)=$\frac{5}{2}$n(MnO4-)=20.4ml×10-3×0.2000mol•L-1×$\frac{5}{2}$=0.0102mol;
故答案为:0.0102mol;
(4)从图象上观察,随着反应对进行,曲线的斜率越来越大,说明单位时间内Mn2+的浓度越来越大,所以反应速率越来越快,反应中温度不变,随着反应的进行,反应物的浓度变小,而反应速率加快,只能是生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快;
故答案为:生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快.
点评 本题主要考查物质的分离、提纯、制备以及反应速率等,综合性比较强,考查学生收集、整合、分析问题的能力,难度有点大.


科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2L N2含有的分子数为0.5NA | |
| B. | 在常温常压下,1mol 氖气含有的原子数为2NA | |
| C. | 27g Al与足量的盐酸反应失去的电子数为3NA | |
| D. | 在同温同压时,相同体积的任何气体单质所含的原子数一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、I-、CO32-、Fe3+ | B. | Na+、Ba2+、Mg2+、HCO3- | ||
| C. | NO3-、Mg2+、Cl-、Ca2+ | D. | K+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
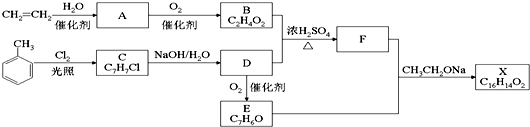
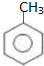 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$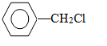 .B和D反应生成F的化学方程式
.B和D反应生成F的化学方程式 .D→E的化学方程式2
.D→E的化学方程式2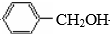 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O.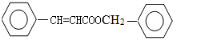 .
.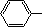 CH2OCH2CH2CHO B.
CH2OCH2CH2CHO B.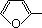 CH=CHCH2CH2CHO
CH=CHCH2CH2CHO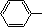 COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.
COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )可生产塑料单体苯乙烯(
)可生产塑料单体苯乙烯(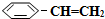 ),其原理反应是:
),其原理反应是: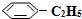 (g)?
(g)?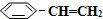 (g)+H2(g)△H=+125kJ•mol-1.
(g)+H2(g)△H=+125kJ•mol-1.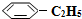 (g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:| 时间/min | 0 | 10 | 20 | 30 | 40 |
n( )/mol )/mol | 0.40 | 0.30 | 0.26 | n2 | n3 |
n(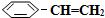 )/mol )/mol | 0.00 | 0.10 | n1 | 0.16 | 0.16 |
 (g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将越大(填“越大”、“越小”或“不变”),原因是体系总压强一定时,水蒸气的分压越大,平衡体系的分压越小,平衡向气体体积增大的方向移动
(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将越大(填“越大”、“越小”或“不变”),原因是体系总压强一定时,水蒸气的分压越大,平衡体系的分压越小,平衡向气体体积增大的方向移动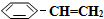 (g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下
(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下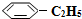 (g)和
(g)和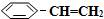 (g)的浓度c随时间t变化的曲线.
(g)的浓度c随时间t变化的曲线.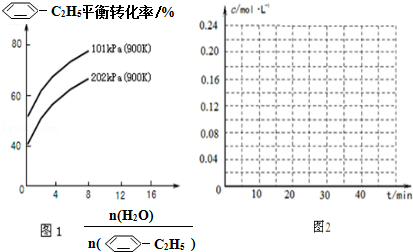
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 已知条件 | 热化学方程式 | |
| A | 中和热为57.3kJ/mol | H2SO4(aq)+Ba(OH)2(aq)═ BaSO4(s)+2H2O(l) △H=-114.6kJ/mol |
| B | 合成氨反应生成0.1mol NH3时放出a kJ热量 | N2(g)+3H2(g)?2NH3(g) △H=-20a kJ/mol |
| C | H2的燃烧热为285.8kJ/mol | H2(g)+$\frac{1}{2}$O2(g)═H2O(g) △H=-285.8kJ/mol |
| D | 碳的燃烧热为393.5kJ/mol | 2C(s)+O2(g)═2CO(g) △H=-787kJ/mol |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com