
【题目】下列说法正确的是( )
A.凡是放热反应的发生均无需加热B.物质发生化学反应都伴随着能量变化
C.凡是需要加热后才能发生的反应是吸热反应D.伴有能量变化的物质变化都是化学变化
科目:高中化学 来源: 题型:
【题目】下列反应都有水参加,其中属于氧化还原反应,而水既不做氧化剂,又不做还原剂的是
A.2F2+2H2O=4HF+O2 B.2Na+2H2O=2NaOH+H2↑
C.C12+H2O=HC1O+HC1 D.C+H2O![]() CO+H2
CO+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+nB(g)![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是
pC(g)的速率和平衡的影响图像如下,下列判断正确的是
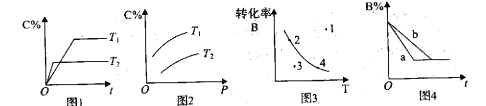
A. 由图1可知,T1<T2,该反应正反应为吸热反应
B. 由图2可知,该反应m+n<p
C. 图3中,点3的反应速率V正>V逆
D. 图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出的有关表述中不准确的是
序号 | A | B | C | D |
物质类型 | 离子化合物 | 共价键直接构成的物质 | 共价分子 | 稀有气体 |
代表物质 | NaCl | 金刚石 | 干冰 | Ne |
组成晶体的结构微粒 | Na+、Cl- | C | CO2 | Ne |
结构微粒间相互作用 | 离子键 | 共价键 | 分子间作用力 | 共价键 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)5 mol的CO2与8 mol的SO2的分子数之比是________;原子数之比是________;质量比是________。
(2)KClO3和浓HCl在一定温度下反应会生成黄绿色的易爆物二氧化氯。其反应可表述为:________KClO3+________HCl(浓)===________KCl+________ClO2↑+________Cl2↑+________H2O
①配平以上化学方程式(化学计量数填入划线上)。
②ClO2是反应的________(填“氧化”或“还原”)产物。浓盐酸在反应中显示出来的性质是(填写号码)________。
a.还原性 b.氧化性 c.酸性 d.碱性
③反应产生0.1 mol Cl2,则转移的电子的物质的量为________ mol。
④ClO2具有很强的氧化性,因此可被用来做消毒剂,若ClO2作消毒剂后其自身转化为Cl-,则其消毒的效率(以单位质量得到电子数表示)是Cl2的________倍(保留2位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.01mol/LNaOH溶液滴定20.00mL0.01mol/LCH 3COOH溶液,所得滴定曲线如右图。下列说法正确的是
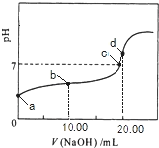
A. b点对应的溶液中: c(OH—)+c(CH3COO—) = c(Na+)+c(H+)
B. a点对应溶液的pH= 2
C. C点表示NaOH溶液与CH3COOH溶液恰好完全反应
D. d点对应的溶液中,水的电离程度小于同温下纯水的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其氧化物是日常生活生产中应用广泛的材料,请回答下列问题:
(1)基态铁原子的价电子排布式为_________。
(2)Fe3+、Co3+与N3+、CN-等可形成络合离子。
①C、N、O中第一电离能最大的为________,其原因是_____________________。
②K3[Fe(CN)6]可用于检验Fe2+,1mol K3[Fe(CN)6]中含有σ键的数目为________________。
(3)铁的另一种配合物Fe(CO)x的中心原子价电子数与配体提供的电子数之和为18,则x=_____。已
知该配合物的熔点为-20.5 ℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)x晶体属于_____________(填晶体类型)。
(4)金属铁晶体中原子采用_________堆积,铁晶体的空间利用率为______(用含π的式子表示)。
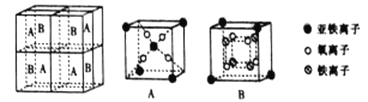
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B 方块组成。则该化合物中Fe2+、Fe3+、O2-的个数比为_______________(填最简整数比);已知该晶体的密度为d g·cm-3,阿伏加德罗常数的值为NA,则晶胞参数a为_______________nm(用含d和NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000mol/L 盐酸滴入20.00mL1.000 mol/L 氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。
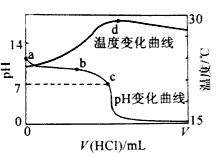
下列有关说法不正确的是( )
A. a 点由水电离出的c(H+)>1.0×10-14mol/L
B. b 点: c(NH4+)>c(Cl-)
C. c 点: c(Cl-)=c(NH4+)
D. d 点后,溶液温度略下降的主要原因是NH3·H2O 电离吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,lmolX与3molY在恒容密闭容器中发生反应X(g)+3Y(g)![]() 2Z(g),△H = -QkJ·mol-1(Q>0),下列说法正确的是( )
2Z(g),△H = -QkJ·mol-1(Q>0),下列说法正确的是( )
A. 达到平衡时,3v正(Y)=2v逆(Z)
B. 反应一段时间后,X与Y的转化率之比为1:3
C. X的体积分数不变,说明反应己达到平衡状态
D. 达到平衡后,若从平衡体系中移走部分的Z则v正增大v逆减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com