

���� ��1����ʵ��I��Һ��ɫ���ٸı�ʱ���ٽ���ʵ��II��Ŀ����ʹʵ��I�ķ�Ӧ�ﵽ��ѧƽ��״̬��
��2������ʵ��iii��ʵ��ii�ĶԱȿ��Կ�����Ϊ���ų���ii��ˮ�����Һ������Ũ�ȸı��Ӱ�죻
��3������AgNO3��Ag+��I-����AgI��ɫ������I-Ũ�Ƚ��ͣ�2Fe3++2I-?2Fe2++I2ƽ�������ƶ���
��4������FeSO4��Fe2+Ũ������ƽ�����ƣ�
��K�պ�ʱ��ָ������ƫת����֪b��Fe3+�õ����ӣ���������
�ڵ�ָ����㣨��Ӧ�ﵽƽ�⣩����U������еμ�0.01mol/L AgNO3��Һ�������ɻ�ɫ��������֪I-Ũ�Ƚ��ͣ�2Fe3++2I-?2Fe2++I2ƽ�������ƶ���
��5����Fe2+Ũ������ԭ����ǿ��
���루4��ʵ��Աȣ���ͬ�IJ����ǵ�ָ����㣨��Ӧ�ﵽƽ�⣩����U���ҹ��еμ�0.01mol/L FeSO4��Һ��
��6������3���ͣ�4������5�����Աȣ���֪�����ԡ���ԭ����Ũ���йأ�
��� �⣺��1����ʵ��I��Һ��ɫ���ٸı�ʱ���ٽ���ʵ��II��Ŀ����ʹʵ��I�ķ�Ӧ�ﵽ��ѧƽ��״̬���������ƽ���ƶ����жϣ��ʴ�Ϊ����ѧƽ��״̬��
��2����ʵ��iii��ʵ��ii�ĶԱȿ�֪���Ա�ʵ���Ŀ����Ϊ���ų���ii��ˮ�����Һ������Ũ�ȸı��Ӱ�죬�ʴ�Ϊ����Һϡ�ͣ�c��Fe2+�����ͣ�
��3������AgNO3��Ag+��I-����AgI��ɫ������I-Ũ�Ƚ��ͣ�2Fe3++2I-?2Fe2++I2ƽ�������ƶ�����֪Fe2+��Fe3+ת����
�ʴ�Ϊ��i��Ag+����I-��Ag+��aq��+I-��aq��?AgI��s����I-Ũ���½���ʹƽ��2Fe3++2I-?2Fe2++I2�����ƶ�����������Fe2+Ũ�ȣ�ͬ��ƽ��2Fe3++2I-?2Fe2++I2�����ƶ���
��4������FeSO4��Fe2+Ũ������ƽ�����ƣ�
��K�պ�ʱ��ָ������ƫת���Ҳ�Ϊ��������֪b��Fe3+�õ����ӣ���b��������
�ʴ�Ϊ������
�ڵ�ָ����㣨��Ӧ�ﵽƽ�⣩����U������еμ�0.01mol/L AgNO3��Һ�������ɻ�ɫ������I-Ũ�Ƚ��ͣ�2Fe3++2I-?2Fe2++I2ƽ�������ƶ���ָ������ƫת��Ҳ��֤���Ʋ�Fe2+��Fe3+ת����
�ʴ�Ϊ�������Һ��ɫ��ɫ���л�ɫ�������ɣ�������ָ������ƫת��
��5����ת����ԭ��ΪFe2+Ũ������ԭ����ǿ��ʹFe2+��ԭ��ǿ��I-���ʴ�Ϊ��Fe2+Ũ������ԭ����ǿ��ʹFe2+��ԭ��ǿ��I-��
���루4��ʵ��Աȣ���ͬ�IJ����ǵ�ָ����㣨��Ӧ�ﵽƽ�⣩����U���ҹ��еμ�0.01mol/L FeSO4��Һ��Fe2+��Fe3+ת����
�ʴ�Ϊ����ָ����������ܵμ�AgNO3��Һ���������ҹܼ���1mL1mol•L-1FeSO4��Һ��
��6������3���ͣ�4������5�����Աȣ��ó��Ľ����Ǹ÷�ӦΪ�����������ԭ��Ӧ����ƽ��ʱ��ͨ���ı����ʵ�Ũ�ȣ����Ըı����ʵ���������ԭ��������Ӱ��ƽ���ƶ���
�ʴ�Ϊ���÷�ӦΪ�����������ԭ��Ӧ����ƽ��ʱ��ͨ���ı����ʵ�Ũ�ȣ����Ըı����ʵ���������ԭ��������Ӱ��ƽ���ƶ���
���� ����Ϊ2015�걱���߿����⣬����ԭ��ء�������ԭ��Ӧ��ƽ���ƶ����ۺϿ��飬����ƽ���ƶ���Ӱ�����ؼ����ʵ�����Ϊ���Ĺؼ����Է�����ʵ������Ҫ��ϸߣ���Ŀ�ѶȽϴ�


 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���a1b1=a2b2��������Һ��pH��7 | |
| B�� | ������Һ��pH=7��������Һ��c��CH3COO-��=c��Na+�� | |
| C�� | ���a1=a2��b1=b2������ҺҺ��c��CH3COO-��=c��Na+�� | |
| D�� | ���a1=a2���һ����Һ��pH��7����b1��b2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ����Ӧ��Ũ�� | B�� | �����¶� | C�� | ����ѹǿ | D�� | ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| t/s | 0 | 500 | 1000 | 1500 |
| c��N2O5��/mol | 5.00 | 3.5 | 2.50 | 2.50 |
| A�� | 500 s��N2O5�ֽ�����Ϊ3��10-4mol•��L•s��-1 | |
| B�� | ��Ӧ��ƽ����������м���5molN2O5���壬ƽ�������ƶ�����Ӧ����ЧӦ��� | |
| C�� | ��ͬ�¶��£���ʼʱ�������г���5molNO2��1.25molO2���ﵽƽ��ʱ��NO2��ת����С��50% | |
| D�� | �ﵽƽ�����ͬ�������������г���2.5molN2O5��1.25molO2����ʱƽ�⽫�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
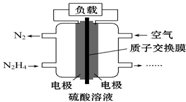 Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С����������洢װ�õ��ŵ㣮һ�����£�N2H4��Ϊȼ�ϵĵ��װ����ͼ��ʾ���õ���ÿ����е�������Ϊ��������H2SO4��Ϊ����ʣ����й��ڸ�ȼ�ϵ�ص�������ȷ���ǣ�������
Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С����������洢װ�õ��ŵ㣮һ�����£�N2H4��Ϊȼ�ϵĵ��װ����ͼ��ʾ���õ���ÿ����е�������Ϊ��������H2SO4��Ϊ����ʣ����й��ڸ�ȼ�ϵ�ص�������ȷ���ǣ�������| A�� | ���������缫�������غ������Ҳ�缫 | |
| B�� | ���������ĵ缫��ӦʽΪN2H4-4e-�TN2��+4H+ | |
| C�� | ���ø�ȼ�ϵ�ع�ҵ�Ͽ��Ե��MgCl2��Һ�Ʊ�Mg | |
| D�� | ��ȼ�ϵ�س����ŵ�ʱ���Ҳ���������缫��Ӧ����H+����c��H+����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��ͼ��ʾ��A��Ԫ�ص��⻯��ķе� | |
| B�� |  ��ͼ��ʾ��A��Ԫ�ص��۵� | |
| C�� |  ��ͼ��ʾNa+��Mg2+��Al3+�İ뾶 | |
| D�� |  ��ͼ��ʾ��������Ԫ�صĵ��ʵ��۵� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com