
| Cl2光照 |
| ① |

| NaOH乙醇 |
| ② |

| Br2的CCl4溶液 |
| ③ |
| ④ |

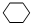 ,反应②发生卤代烃的消去反应生成环己烯,反应③是环己烯与溴发生加成反应生成B为
,反应②发生卤代烃的消去反应生成环己烯,反应③是环己烯与溴发生加成反应生成B为 ,反应④发生卤代烃的消去反反应生成
,反应④发生卤代烃的消去反反应生成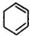 .
. ,反应②发生卤代烃的消去反应生成环己烯,反应③是环己烯与溴发生加成反应生成B为
,反应②发生卤代烃的消去反应生成环己烯,反应③是环己烯与溴发生加成反应生成B为 ,反应④发生卤代烃的消去反反应生成
,反应④发生卤代烃的消去反反应生成 .
. ,名称为环己烷,故答案为:
,名称为环己烷,故答案为: ;环己烷;
;环己烷; ,分子式是C6H10Br2,故答案为:
,分子式是C6H10Br2,故答案为: ;C6H10Br2;
;C6H10Br2;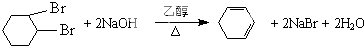 ,
, .
.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅酸钠的水溶液俗称水玻璃,可用作木材防火剂 |
| B、开发核能、太阳能等新能,推广基础甲醇汽油,使用无磷洗涤剂都可直接降低碳排放 |
| C、在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 |
| D、汽车尾气中含有氮的氧化物,是汽油不完全燃烧造成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 叙述 | 推论 | |
| A | 酸性:HCl>H2CO3>H2SiO3 | 非金属性:Cl>C>Si |
| B | 组成原电池时,通常是还原性较强的物质做负极 | 镁和铝在氢氧化钠溶液中组成原电池时,镁做负极 |
| C | -OH是亲水基,含有-OH的有机物都易溶于水 | 常温时,C2H5OH和  都易溶于水 都易溶于水 |
| D | 溶解度小的沉淀可转化成溶解 度更小的沉淀 | 向AgCl悬浊液中滴加KI溶液可以得到AgI沉淀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 7 |
| 2 |
| A、通氧气的电极为正极 |
| B、参加反应的O2与C2H6的物质的量之比为7:2 |
| C、放电一段时间后,KOH的物质的量浓度将下降 |
| D、在电解质溶液中OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 电化学原理在医学医疗中有重要应用.
电化学原理在医学医疗中有重要应用.查看答案和解析>>
科目:高中化学 来源: 题型:
| H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.01mol?L-1 |
| B、0.017mol?L-1 |
| C、0.05mol?L-1 |
| D、0.50mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com