
| A、6.4 g铜粉与足量硫粉充分反应,失去的电子数为0.2 NA |
| B、Na2O2与足量H2O反应生成0.2molO2,转移电子的数目为0.4 NA |
| C、标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2 NA |
| D、0.5 mol?L-1CuCl2溶液中含有Cu2+数小于0.5 NA |


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
| A、③⑥ | B、③④ | C、②③ | D、②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法正确的是( )
用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法正确的是( )| A、燃料电池工作时,电极b作负极 |
| B、工作时,电流由负极通过传感器流向正极 |
| C、b电极的电极反应式为:O2+2H2O+4e-═4OH- |
| D、当消耗11.2L(标准状况下)CO时,理论上传感器中会通过NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
 | ||
B、某有机物的分子的简易球棍模型如图,分子式为C3H7O2N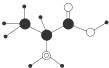 | ||
C、羟基乙酸(HOCH2COOH)的缩聚物: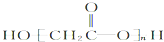 | ||
| D、铁在元素周期表中位于第4周期第ⅧB 族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,56g乙烯和丙烯的混合气中含有的碳原子数为4NA |
| B、156g Na2O2固体与足量的二氧化碳反应时,转移的电子数为4NA |
| C、将1.06克Na2CO3固体溶于水,溶液中含CO32-数目为0.01NA |
| D、标准状况下,向溶有2.24LSO2的水溶液中,通入3.36LCl2,转移电子数目0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCO3-+H+═CO2↑+H2O |
| B、HCO3-+OHˉ═CO32-+H2O |
| C、HCO3-+H2O═H3O++CO32- |
| D、HCO3-+H2O?H2CO3+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 事实 | 解释 |
| A | 用pH试纸测出新制氯水的pH为3 | 新制氯水有酸性 |
| B | C2H5OH与浓硫酸170℃共热,制得的气体使酸性KMnO4溶液褪色 | 一定是制得的乙烯使酸性KMnO4溶液褪色 |
| C | 收集铜与浓硝酸反应生成的气体,用冰水混合物冷却降温,气体颜色变浅 | 生成的红棕色NO2气体部分转化为无色气体 |
| D | 甲苯能使酸性高锰酸钾溶液褪色 | 发生了萃取 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com