
(6分)
已知:Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,能氧化浓HCl生成Cl2;PbO2不稳定,随温度升高按下列顺序逐步分【解析】
PbO2→Pb2O3→Pb3O4→PbO。
现将amol PbO2加热分解,收集产生的O2;向加热后所得固体中加入足量的浓盐酸,收集产生的Cl2。加热反应后所得固体中,Pb2+占Pb元素的物质的量分数为x;两步反应中收集的O2和Cl2的物质的量之和为y mol。
试回答下列问题:
⑴试写出Pb2O3与浓盐酸反应的化学方程式__________________________
⑵通过计算确定y与a、x的函数关系式____________________
⑶若两步反应中O2和Cl2的物质的量之比为5∶3,则剩余固体中含有的物质为____;其物质的量之比为________________。
(1)Pb2O3+6HCl =2PbCl2+Cl2+3H2O
(2)y=(1—0.5x)a (3)Pb3O4 PbO 3:4
【解析】
试题分析:(1)Pb的化合价有+2、+4,+4价的Pb具有强氧化性,能氧化浓HCl生成Cl2,本身被还原为+2价的Pb,根据元素守恒得反应物与生成物并根据化合价升降法配平即得。
(2)根据题意得:1mol PbO2分解得到的混合物中n Pb2+=x mol,n Pb4+=(1-x)mol。
在反应过程中1mol PbO2中Pb4+全部降低为Pb2+,
根据得失电子守恒:n(O2)=2x/4×a=0.5xa mol,
再与足量的浓盐酸反应生成氯气,得n(Cl2)=a×[(1-x) ×2/2]= a(1-x) mol,
y = n(O2)+ n(Cl2)= (1—0.5x)a
(3) 若两步反应中O2和Cl2的物质的量之比为5∶3,带入(2)中式子可得x=10/13,则剩余固体中Pb2+的物质的量的分数为10/13,Pb4+的物质的量分数为3/13,即n Pb2+/ n Pb4+=10:3。
由题意,PbO2不稳定逐步分解顺序:PbO2→Pb2O3→Pb3O4→PbO.因为Pb的化合价只有+2、+4,所以Pb2O3可表示为PbO?PbO2,Pb3O4可表示为2PbO?PbO2,各氧化物中n(pb2+):n(pb4+)的比值关系为:
PbO2中,n(pb2+):n(pb4+)═0:1
Pb2O3中,n(pb2+):n(pb4+)═1:1
Pb3O4中,n(pb2+):n(pb4+)═2:1
PbO中,n(pb2+):n(pb4+)═1:0
根据剩余固体中n(pb2+):n(pb4+)═10:3,介于3:1和4:1之间,所以此时剩余固体包括Pb3O4、PbO两种物质
设剩余固体中Pb3O4物质的量为a、PbO物质的量为b,
得n(pb2+)═2a+b,n(pb4+)═a,
则(2a+b):a═10:3
解得a:b═3:4,即Pb3O4:PbO=3:4,
故答案为:Pb3O4、PbO;3:4.
考点:常见金属单质及化合物的性质的综合运用。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014湖南师大附中第二学期期中考试高一化学试卷(解析版) 题型:选择题
与氢氧根具有相同的质子数和电子数的微粒是
A.CH4 B.NH4+ C.NH2- D.Cl-
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省高一下学期期中联考化学试卷(解析版) 题型:填空题
(6分)有下列七种物质:①Cl2 ②Na2O2 ③H2O2 ④NH4Cl ⑤CH4 ⑥NaHSO4 ⑦Ne
回答下列问题
(1)不存在化学键的是_______________;(填序号)
(2)含有极性键和非极性键的是_______________;(填序号)
(3)NaHSO4固体溶于水,破坏了_____________键;其电离方程式为______________________
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉市高三四月调考理综化学试卷(解析版) 题型:简答题
(15分)
亚硝酸钠(NaNO2)易溶于水,微溶于乙醚,是常用的食品发色剂
(1)第一电离能:N ___O(填“<”、“>”或“=”);NO2-的空间构型为____
(2)亚硝酸钠在3200C会分解生成氧化钠、一氧化二氮等物质,该反应的化学方程式为____
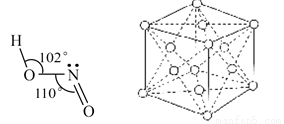
(3)亚硝酸钠是亚硝酸的钠盐。HNO2的结构如图所示,则HNO2分子中有___个 键:
键:
HNO2的酸性比HN03弱是因为_____
(4)亚硝基钻钠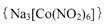 是钴的一种配合物,易溶于水,与钾离子反应生成淡黄色的
是钴的一种配合物,易溶于水,与钾离子反应生成淡黄色的
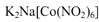 沉淀,可用于检验K+的存在。
沉淀,可用于检验K+的存在。
①基态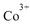 的价层电子排布图为_____
的价层电子排布图为_____
②用亚硝酸钻钠检验K+的离子方程式是
③金属钴的堆积方式如图所示,若一个钴原子的半径为r,,则晶胞的体积V(晶胞)=__
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉市高三四月调考理综化学试卷(解析版) 题型:选择题
在盛有足量M的体积可变的密闭容器中加入N,发生反应:M (s) +2N (g)==4P (s) +Q (g) ΔH< 0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是

A.平衡是N的转化率为50%
B.当温度升高后,则图中θ>450
C.若再加入N,则正、逆反应速率均逐渐增大
D.若再加入N,则反应体系中气体密度减小
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉外国语学校高一下学期期中考试化学试卷(解析版) 题型:选择题
将15.6gNa2O2和5.4gAl同时放入一定量的水中,充分反应后得到200mL澄清溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则
A.反应过程中得到6.72L的气体(标准状况下)
B.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-)
C.最终得到7.8g的沉淀
D.最终得到的溶液中c(NaCl)=1.6 mol/L
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉外国语学校高一下学期期中考试化学试卷(解析版) 题型:选择题
C、CO、CH4、C2H5OH是常用的燃料,他们每1mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为393.5kJ、283.0 kJ、890.3 kJ、1366.8 kJ。相同质量的这4种燃料,完全燃烧时放出热量最多的是:( )
A.C B. CO C. CH4 D. C2H5OH
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省宜昌市高三5月模拟理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大
B.1 mol·L-1的NH4Cl溶液中含有NH4+的数目一定小于NA
C.用石墨电极电解FeCl3溶液,阴极反应:2Fe3++6H2O+6e-=2Fe(OH)3↓+3H2↑
D.将带有相反电荷的胶体混合,一定会出现胶体聚沉现象
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省四校下学期期中考试高一化学试卷(解析版) 题型:选择题
为探究锌与稀盐酸反应速率[以v(H2)表示],向反应混合液中加入某些物质,下列判断正确的是
A.加入铜粉,v(H2) 增大
B.加入NaCl固体,会增大Cl—浓度,从而使v(H2)增大
C.加入NaHSO4固体v(H2)不变
D.加入水,锌不与水反应,v(H2)不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com