
【题目】已知:①2CO(g)+O2(g)=2CO2(g) ΔH=-568kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g) ΔH=-248kJ·mol-1
已知 CO 和 H2 的混合物 1 mol 在氧气中充分燃烧放出的热量 272 kJ,则该混合气体中 CO 和氢气的物质的量的比值为
A.1∶1 B.3∶37 C.2∶1 D.3∶2
 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】常温下,将0.1mol/L的氢氧化钠与0.06mol/L硫酸溶液等体积混合,该混合溶液的pH等于( )
A.1.7 B.2.0 C.12.0 D.12.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一份含有FeCl3和FeCl2固体混合物,为测定各成分的含量进行如下两个实验:
实验1:① 称取一定质量的样品,将样品溶解;
② 向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀;
③ 将沉淀过滤、洗涤、干燥得到白色固体17.22 g。
实验2:① 称取与实验1中相同质量的样品,将样品溶解;
② 向溶解后的溶液中通入足量的Cl2;
③ 再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀;
④ 将沉淀过滤、洗涤后,加热灼烧,到质量不再减少,得到固体物质4g。
回答下列问题:
(1)溶解过程中所用到的玻璃仪器有___________________。
(2实验室保存FeCl2溶液时通常会向其中加入少量试剂_____________和_____________。
(3)实验2通入足量Cl2的目的是_____________;涉及的化学反应的离子方程式是____________________。
(4检述实验2的步骤④中沉淀已经洗涤干净的方法是_____________。
(5)加热FeCl3溶液,并将溶液蒸干时,通常不能得到FeCl3固体,请以平衡的观点解释其原因(方程式与文字相结合来说明)______________________。
(6)FeCl3溶液可以用于止血,主要是因为FeCl3溶液能使血液聚沉,这涉及胶体的特性。以下关于胶体的说法不正确的是_____________。
A.胶体粒子能透过滤纸,但不能透过半透膜
B.胶体粒子具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象
C.向Fe(OH)3胶体可以产生丁达尔效应,CuSO4溶液、水等分散系不能产生丁达尔效应
D.向Fe(OH)3胶体中滴加硫酸,会先出现红褐色沉淀,随后沉淀消失
E.在蛋白质溶液中加入稀的CuSO4溶液,可使蛋白质盐析
(7)通过实验所得数据,计算固体样品中FeCl3和FeCl2的物质的量之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学小组用实验的方法进行探究影响化学反应速率的因素。
他们只利用Cu、Fe、Al和不同浓度的硫酸(0.5mol·L-1、2mol·L-1、18.4mol·L-1)。设计实验方案来研究影响反应速率的因素。甲同学研究的实验报告如下表:

(1)甲同学表中实验步骤②为__________________
(2)甲同学的实验目的是__________________
(3)乙同学为了更精确的研究浓度对反应速率的影响,利用下图所示装置进行定量实验。

乙同学在实验中应该测定的数据是______________
(4)乙同学完成该实验应选用的实验药品是________________;该实验中不选用某浓度的硫酸,理由是______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
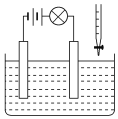
A.盐酸中逐滴加入食盐溶液
B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中逐滴加入稀盐酸
D.硫酸中逐滴加入氢氧化钡溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】〔化学—选修3:物质结构与性质〕
早期发现的一种天然准晶颗粒由三种Al、Cu、Fe元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过 方法区分晶体、准晶体和非晶体。
(2)基态铁原子有 个未成对电子,三价铁离子的电子排布式为: 可用硫氰化钾奉验三价铁离子,形成配合物的颜色为 。
(3)新制备的氢氧化铜可将乙醛氧化为乙酸,而自身还原成氧化亚铜,乙醛中碳原子的杂化轨道类型为 ;一摩尔乙醛分子中含有的σ键的数为: 。乙酸的沸点明显高于乙醛,其主要原因是: 。氧化亚铜为半导体材料,在其立方晶胞内部有四个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
(4)铝单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为 。列式表示铝单质的密度 g·cm-3(不必计算出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1mol/LNaOH溶液450mL和 0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是____________。(填序号)仪器C的名称是________,苯实验所需玻璃仪器E规格和名称是___________。
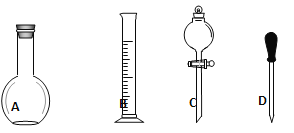
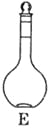
(2)下列操作中,容量瓶所不具备的功能有__________(填序号)
A.配制一定体积准确浓度的标准溶液 | B.长期贮存溶液 |
C.用来加热溶解固体溶质 | D.量取220毫升体积的液 |
(3)在配制NaOH溶液实验中,共它操作均正确,若定容时仰视刻度线,则所配制溶溶液浓度_____________0.1mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度__________0.1mol/L。
(4)根据计算得知:所需质量分数为98%、密度为1.84g.cm-3的浓硫酸的体积为__________mL(计算结果保留一位小数)。如果实验室有l0mL、25mL、50mL量筒,,应选用__________mL规格的量筒最好。
(5)如果定容时不小心超过刻度线,应如何操作___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com